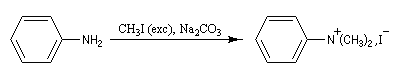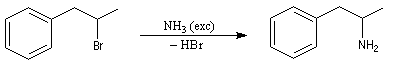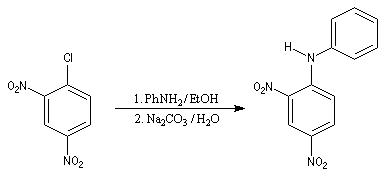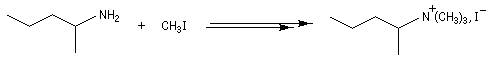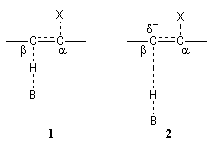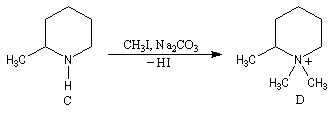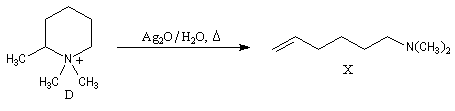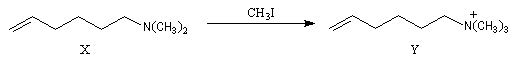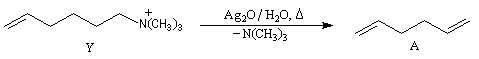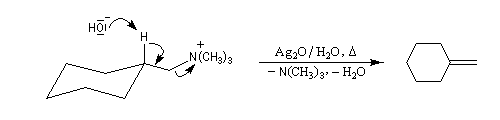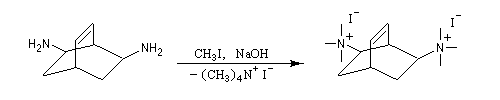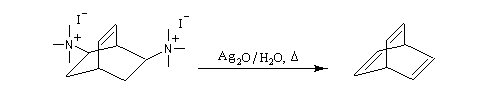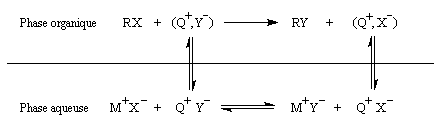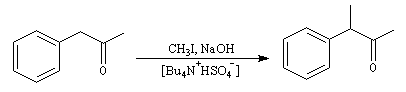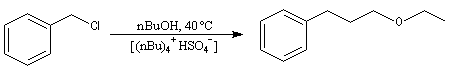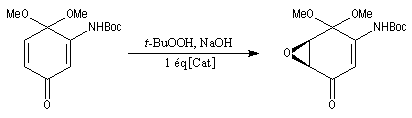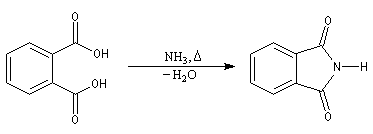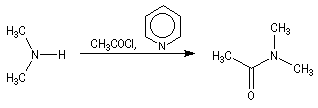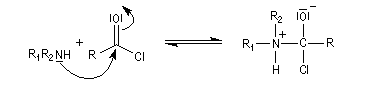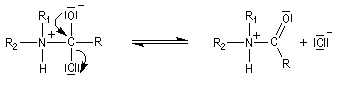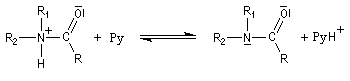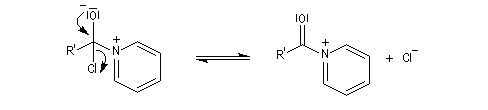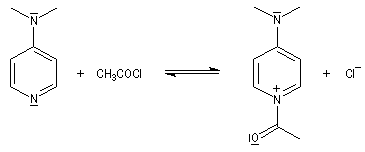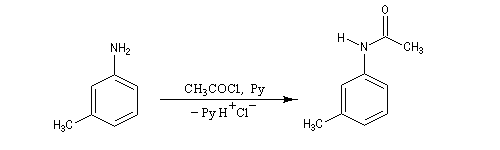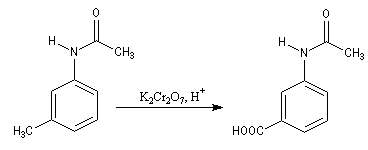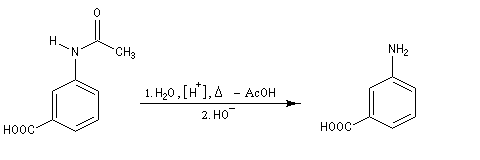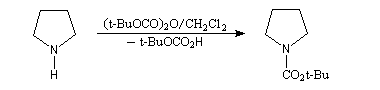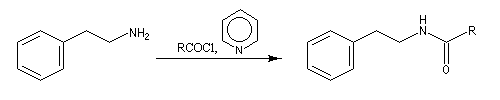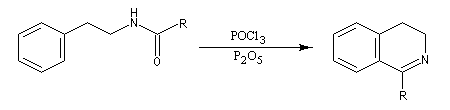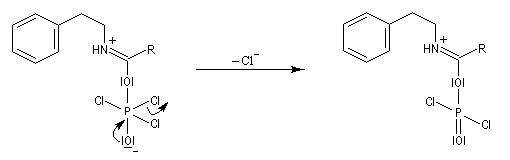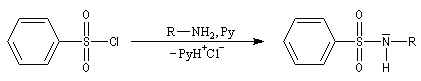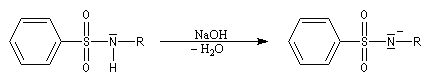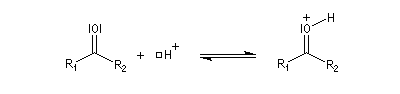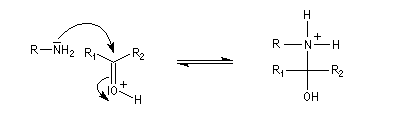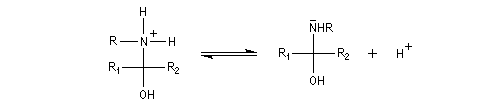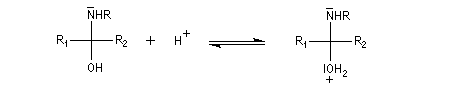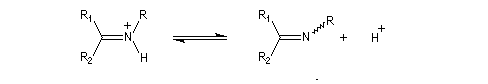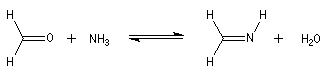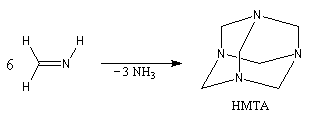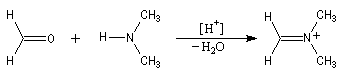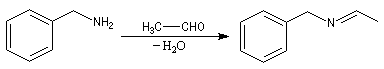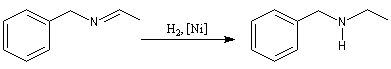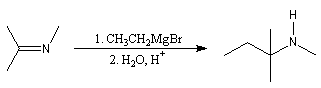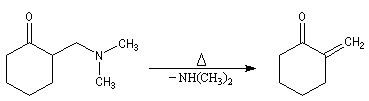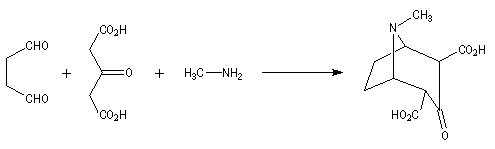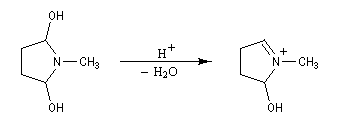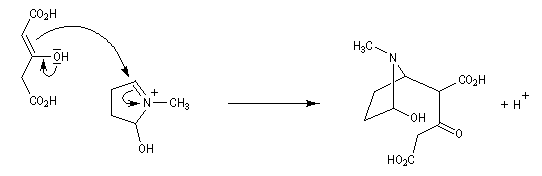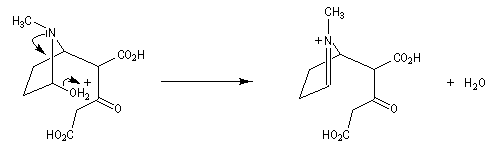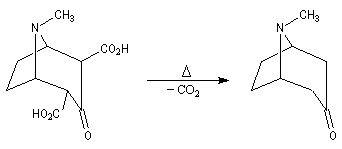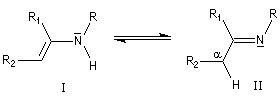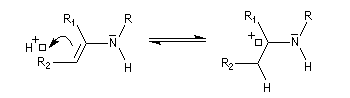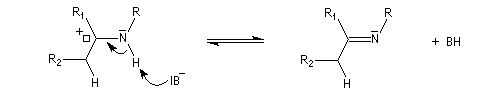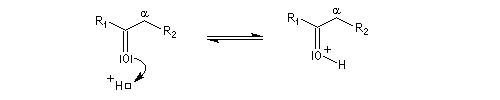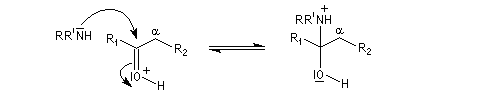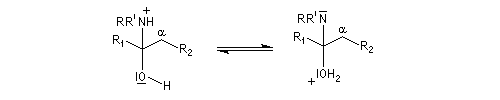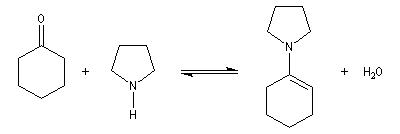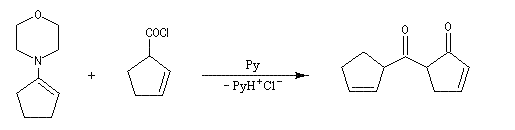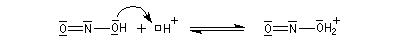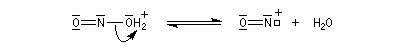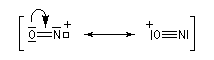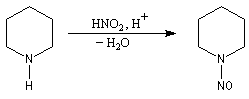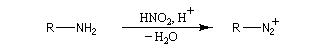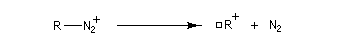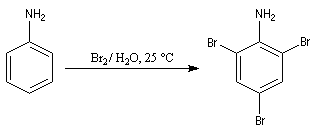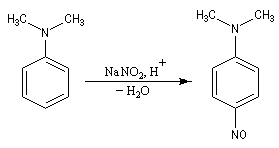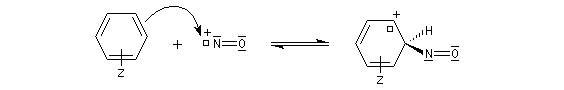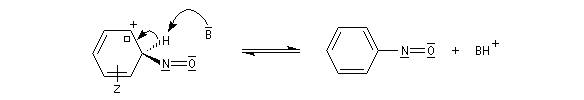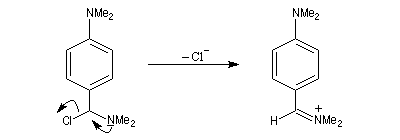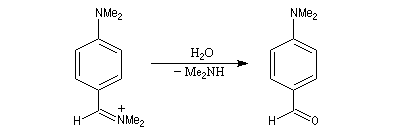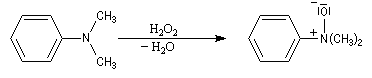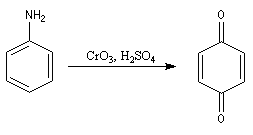Cours de chimie Organique - G. Dupuis - Lycée Faidherbe de Lille
Amines et composés apparentés
Introduction
Classe
Les amines sont des composés azotés qui dérivent formellement de l'ammoniac NH3 par remplacement d'un ou plusieurs atomes d'hydrogène par des groupes carbonés.
Le nombre n des atomes d’hydrogène liés à l'azote, définit la classe de l’amine. Leur découverte est due au chimiste allemand Wurtz en 1849.
|
n |
2 |
1 |
0 |
|
Classe |
primaire |
secondaire |
tertiaire |
On notera la différence entre la définition de la classe des amines et celle des alcools pour lesquels on s’intéresse aux atomes d’hydrogène liés à l’atome de carbone fonctionnel.
La fonction amine recouvre un ensemble très étendu de composés. On distingue plusieurs séries :
- Acyclique : l'atome d'azote est relié à un ou plusieurs groupes alkyles. Exemple : la méthylamine CH3
NH2.
Alicyclique : l'atome d'azote est lié à un cycle non aromatique. Exemple : la cyclohexylamine.

Aromatique : l'atome d'azote est lié à un cycle aromatique. Exemple : la phénylamine ou aniline.
Hétérocyclique : l'atome d'azote est engagé dans un cycle qui peut être ou non aromatique. Exemples :
|
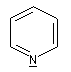
|
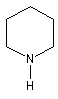
|
|
pyridine |
pipéridine |
Amines acycliques
Les amines acycliques forment des série homologues appartenant aux trois classes. Les amines et des diamines simples qui sont assez volatiles possèdent une odeur souvent nauséabonde. Celle de la triméthylamine rappelle le poisson pourri. La pentane-1,5-diamine qui se forme lors de la décomposition des protéines s'appelle vulgairement cadavérine.
Bases puriques et pyrimidiques
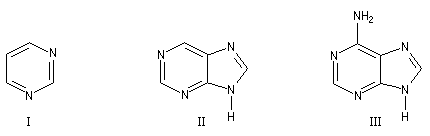
Les bases pyrimidiques et puriques, dérivées respectivement de la pyrimidine (I), de la purine (II), sont des constituants des acides nucléiques. L'adénine (III), intervient
dans la structure de l'ATP.
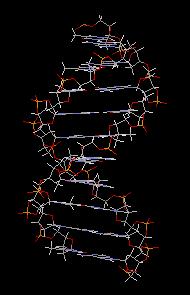
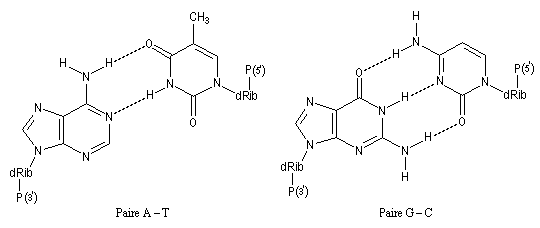
La structure en double hélice de l'ADN (hélice de type B ci-dessous) est assurée grâce à l'appariement de paires de bases par l'intermédiaire de liaisons hydrogène. Adénine-thymine d'une part guanine-cytosine d'autre part. Le schéma ci-dessous représente l'appariement de "type Watson et Crick." La tautomérie céto-énolique (thymine) ou la tautomérie imine-énamine (adénine), jouent un rôle important. En effet, selon les tautomères, les bases peuvent former des liaisons H différentes.
|
|
James Watson, Francis Crick ont proposé la structure en double hélice de l'ADN dans un célèbre article de la revue Nature en 1953 [47]. Leur argumentation s'appuyait notamment sur les travaux de diffraction aux rayons X de Maurice H. F. Wilkins et Rosalind Elsie Franklin (King's College
, Londres.) [39]. Watson, Crick et Wilkins ont obtenu le prix Nobel de physiologie et médecine en 1962. [30]. Compléments sur les propriétés physico-chimiques de l'ADN [22]. (photographie G. D. 2011.)
|
Alcaloïdes
Les molécules hétérocycliques, azotées, d'origine naturelle s'appellent alcaloïdes en raison de leurs propriétés basiques. Ils possèdent généralement une activité biologique marquée. Donnons quelques exemples d'alcaloïdes.
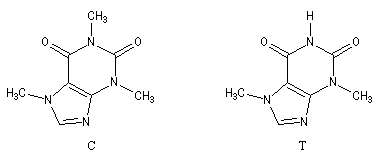
- La caféine (C) peut être extraite du café et du thé [2] et [5]. La théobromine (T) est contenue dans le cacao.
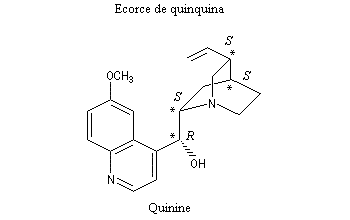
- La quinine, présente dans l'écorce de quinquina, a été le premier médicament réellement efficace contre le paludisme. Malheureusement la toxicité du composé limite son champ thérapeutique. On le réserve dans le traitement de certaines formes aigües qui résistent aux autres antimalariques.
|

|
La découverte des vertus thérapeutiques des dérivés du quinquina remonte au 17ème siècle. La légende veut que la comtesse de Chinchona, femme d'un Roi du Pérou, ait été guérie d'une fièvre (due à la malaria ?) grâce à des décoctions d'écorce de cet arbre.
Le principe actif a été isolé par deux pharmaciens français en 1820, Pierre-Joseph Pelletier et Joseph-Bienaimé Caventou.
En 1908, P. Rabe établit la formule brute correcte de la quinine :
C20H24N2O2.
En 1856, l'impétueux William Perkin, âgé de seulement 18 ans, tente de synthétiser la quinine afin de soigner les combattants britanniques victimes de la malaria en Inde. Se fondant sur la formule brute de la quinine, il recherche des substrats susceptibles de l'engendrer. Considérant l'allyltoluidine comme un bon candidat, il envisage son oxydation selon :
2 C10H13N + O2 =
C20H24N2O2 + H2O
Inutile de dire qu'il ne parvient pas à ses fins. Mais cet échec le conduit à la découverte du premier colorant synthétique : la mauvéine. Il fonde une entreprise afin de commercialiser sa découverte. C'est le début de l'industrie des colorants [19].
La première synthèse stéréosélective de la quinine a été publiée en 2001 par Gilbert Stork (Columbia University).
La molécule possède quatre centres chiraux.
Par exemple : la quinine et la quinidine sont des diastéréo-isomères qui diffèrent par la configuration du centre chiral porteur du groupe OH.
Notons que la quinine fait partie des molécules naturelles du fonds chiral (chiral pool en anglais). A ce titre, elle est utilisée, ainsi que ses dérivés, comme auxilliaire chiral dans plusieurs réactions énantiosélectives. La plus célèbre étant la dihydroxylation asymétrique de Sharpless.
|
La première synthèse formelle de la quinine a été publiée en 1944 par R. B. Woodward et W. Doering. Elle conduisait en réalité à la quinotoxine. Mais Woodward et Doering se sont appuyés sur les travaux de Rabe et Kindler qui avaient montré en 1918 la possibilité de passer de la quinotoxine à la quinine en trois étapes. La faisabilité de cette synthèse a été l'objet de controverses, le point faible étant le travail antérieur de Rabe non reproduit par Woodward. Ce n'est qu'en 2006 que ce débat a été définitivement tranché [36].
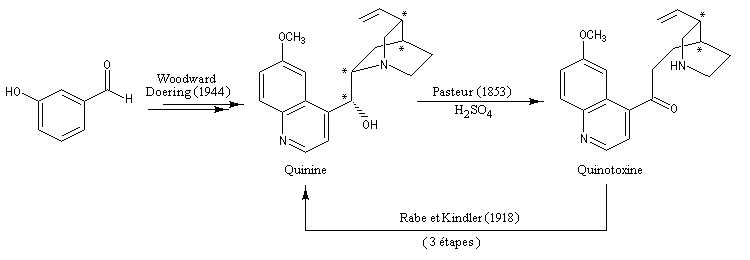
Plusieurs synthèses totales de la quinine ont été publiées : Stork (2001), Jacobsen (2004), Kobayashi (2004). Les grandes lignes de ces synthèses sont données à la référence : [35].
Remarque : la quinine possède la propriété d'être fluorescente sous l'action d'un rayonnement UV de longueur d'onde voisine de 350 nm. La fluorescence s'effectue dans le visible aux alentours de 450 nm. Cette propriété permet son dosage [44].
Le professeur R. B. Woodward (Université de Harvard) est considéré comme l'un des chimistes organiciens les
plus brillants du 20 ème siècle. Le prix Nobel de chimie lui a été attribué en 1965 pour l'ensemble de ses travaux de synthèse organique et notamment la synthèse totale de nombreux composés complexes d'origine naturelle.
Parmi les nombreuses anecdotes qui émaillent la carrière de ce chimiste hors du commun, signalons simplement qu'il conçut les grandes lignes de la synthèse de la quinine alors qu'il était encore jeune élève au lycée. R. B. Woodward est décédé en 1979 [21], [25].
- Certains alcaloïdes sont des poisons violents. La strychnine et la brucine sont présentes à l'état naturel dans la noix vomique. Elles ont été utilisées
comme poison de flèche. L' acide lysergique et ses dérivés sont des composés très toxiques produits par l'ergot de seigle. La coniine est un dérivé de la pipéridine.
|
|
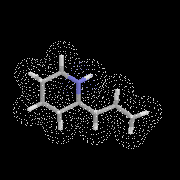
La coniine est la 2-propylpipéridine. A. Ladenburg a séparé les deux énantiomères en 1886. La (S)-(-)-coniine est l'un des alcaloïdes
de Cicuta naculata une ombellifère plus connue sous le nom de cigüe. On la trouve dans la nature le long des chemins. Ce poison était utilisé par
les grecs pour exécuter les condamnés à mort. C'est après avoir absorbé une solution de cigüe que le philosophe Socrate, mourut en - 399 [17].
|
- La strychnine et la brucine sont des amines tertiaires chirales. Elles peuvent être obtenues assez facilement sous forme énantiopure. C'est la raison pour laquelle ont les utilise
comme agents résolvants ou comme auxiliaire chiral dans certaines synthèses asymétriques.
- La dihydroquinine (DHQ) et la dihydroquinidine (DHQD) entrent dans la composition de catalyseurs asymétriques permettant la dihydroxylation énantiosélective des doubles liaisons éthyléniques, réaction mise au point par K. B. Sharpless en 1987.
- La spartéine, un alcaloïde présent à l'état naturel dans le lupin blanc, constitue un ligand chiral dans les réactions de déprotonation énantiosélectives par des organolithiens.
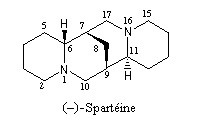
- Par hydrolyse des alcaloïdes, on obtient souvent des molécules plus simples. L'hydrolyse de l'atropine, composé existant dans certaines plantes de la famille des solanacées fournit le tropan-3-ol, achiral (composé méso) et le mélange racémique des acides tropiques (3-hydroxy-2-phénylpropanoïques.)
- De nombreuses toxines possèdent dans leur molécule une ou plusieurs fonctions amine. La tétrodotoxine est présente à l'état naturel chez plusieurs animaux et notamment dans
le poisson tétrodon. Les cuisiniers japonais doivent être titulaire d'un diplôme spécial pour préparer ce plat très apprécié au pays du Soleil levant mais qui provoque plusieurs intoxications mortelles chaque année. C'est en effet l'un des poisons les plus violents connus. Sa structure a été déterminée conjointement par R. B. Woodward et
T. Kishi en 1965. Une monographie consacrée à cette molécule se trouve à la référence [15].
- La morphine est l'un des antalgiques les plus puissants connus.
Quelques amines importantes industriellement
Méthylamine
|
|
La méthylamine est préparée par alkylation de l'ammoniac.
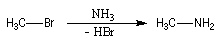
La méthylamine est utilisée comme solvant et comme matière première dans la synthèse de colorants et d'insecticides. |
Ethylamine
|
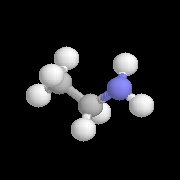
|
L'éthylamine est préparée industriellement par amination réductive de l'éthanal.
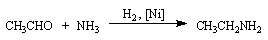
On l'utilise comme solvant dans l'industrie du pétrole et en synthèse organique. . |
Aniline
|
|
C'est l'amine aromatique la plus importante. On l'obtient par réduction du nitrobenzène [6] par un métal en
milieu acide.
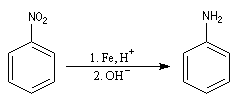
C'est un produit de base de l'industrie des colorants. |
Nomenclature
La méthode qui consiste à considérer une amine comme un dérivé substitué du nitrure d'hydrogène correspondant, appelé azane (l'ammoniac NH3 est l'azane le plus simple), n'est presque jamais employée [40].
Nomenclature radico-fonctionnelle
On ajoute la terminaison amine au nom du groupe lié à l'atome d'azote. L'atome de carbone lié à l'azote porte le numéro 1.
|

|
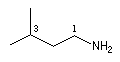
|
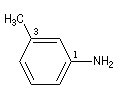
|
|
propylamine |
3-méthyl-1-butylamine |
3-méthyl-1-phénylamine |
- Amines secondaires et tertiaires
On distingue les molécules symétriques et celles qui ne le sont pas. Les composés symétriques sont nommés en faisant précéder
le nom du groupe par un préfixe di, tri etc.
|
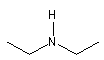
|
|
|
diéthylamine |
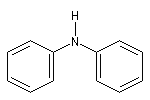
diphénylamine |
Les composés non symétriques sont nommés comme des amines primaires substituées sur l'atome d'azote. Le groupe le plus long ou le plus complexe est choisi pour constituer le nom de l'amine primaire. Les autres, précédés de la lettre N,
sont énoncés dans l'ordre alphabétique.
|
|
|
|
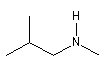
N-méthyl-2-méthylpropylamine |
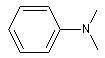
N, N-diméthylphénylamine |
La présence de l'atome d'azote est indiquée par le préfixe aza.
|
|
|
|
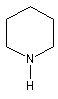
azacyclohexane |
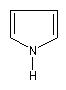
1-azacyclopenta-2,4-diène |
Beaucoup d'amines, notamment les amines hétérocycliques possèdent des noms usuels consacrés par l'usage : la phénylamine est appelée couramment aniline. Le 1-aza-cyclopenta-2,4-diène est appelé pyrrole.
Nomenclature substitutive
On ajoute la terminaison amine au nom de l'alcane après avoir supprimé la lettre e.
|
|

|
|
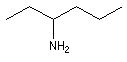
hexan-3-amine |
hexane-1,6-diamine |
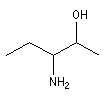
Lorsqu'il n'est pas prioritaire, le groupement NH2 est désigné par amino.
|
|
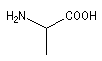
|
|
3-aminopentan-2-ol |
acide 2-aminopropanoïque |
La pyridine et le pyrrole sont des amines hétérocycliques aromatiques citées dans le chapitre sur les composés aromatiques.
Propriétés physiques
Température de changement d'état
Les propriétés physiques sont influencées par l'existence de liaisons hydrogène qui possèdent toutefois une intensité moindre que chez les alcools de masse molaire comparable car l'atome d'azote est moins électronégatif que l'atome d'oxygène. Les amines de faible masse molaire sont miscibles à l'eau.
|
Composé |
M (g.mol-1) |
TE (°C) |
m (D) |
(20 °C, 1 bar) |
|
CH 3CH2OH |
46 |
78,5 |
1,71 |
liq |
|
CH 3CH2NH2 |
45 |
16,6 |
1,29 |
gaz |
Structure
- Amines acycliques et alicycliques
L'atome d'azote est au sommet d'une pyramide y compris dans l'aniline ce qui est conforme aux prévisions de la méthode VSEPR. L'angle a
entre les liaisons est tel que a
< 109° du fait de la présence du doublet non liant.
Dans la plupart des cas, la structure n'est pas rigide. La barrière énergétique séparant les configurations est généralement faible et la fréquence d'interconversion est très élevée.
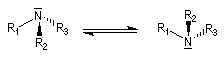
Les valeurs suivantes sont approximatives :
|
E (kJ.mol-1) |
n (MHz)
|
|
30 |
103 |
La hauteur de la barrière d'interconversion peut être déterminée en utilisant la spectroscopie de RMN lorsque la molécule possède des
atomes d'hydrogène diastéréotopiques qui s'interconvertissent lors du phénomène d'inversion comme dans la
dibenzylméthylamine.
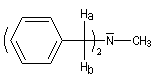
L'inversion de l'azote peut être impossible pour des raisons structurales. Lorsque la molécule est chirale, les deux énantiomères peuvent être séparés. Le premier exemple de ce type concerne la base de Tröger. Le mélange racémique des deux énantiomères a été dédoublé par Prelog et Williams en 1944. Dans cette molécule, la présence d'un système bicyclique interdit la racémisation.
L'inversion peut quelquefois être assez lente pour que
les deux énantiomères puissent être identifiés, voire piégés, à condition d'opérer à une température suffisamment basse. On rencontre ce type de situation dans la famille des aziridines substituées à l'azote.
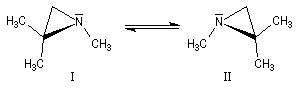
Les ions ammonium quaternaires peuvent être obtenus à partir des amines grâce à la réaction d'alkylation d'Hofmann. Les énantiomères peuvent être séparés et isolés.
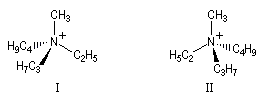
Il en est de même pour les oxydes d'amines chiraux.
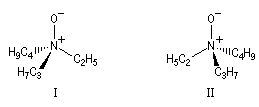
En revanche, les sels d'amines tertiaires sont indédoublables en raison de l'existence d'un équilibre rapide entre l'amine et l'ion aminium.
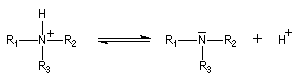
Le cas des amines aromatiques est plus complexe car des effets stériques et électroniques coexistent. L'atome d'azote de l'aniline est au sommet d'une pyramide très aplatie. Le doublet non liant de l'atome d'azote de l'aniline
est engagé dans la résonance avec le cycle aromatique comme en témoigne le sens du moment dipolaire qui est dirigé du cycle vers l'atome d'azote et la
valeur de l'énergie de résonance de la molécule.
|
E R (kJ.mol-1) |
m (D) |
|
172 |
1,56 |
On peut rendre compte de la structure électronique de l'aniline à partir des formes mésomères suivantes :
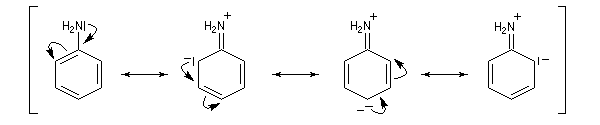
Spectroscopie
Spectroscopie infrarouge
La spectroscopie infrarouge constitue une méthode de choix pour l'identification des structures azotées. Les amines primaires et secondaires peuvent en général être distinguées car elles possèdent
des spectres assez caractéristiques.
|
s (cm-1 ) |
3500 - 3400 |
1650 - 1550 |
1350 - 1250 |
|
Vibration |
élongation N-H (doublet) |
déformation N-H |
élongation C-N |
Rappelons que chez les alcools la vibration d'élongation de la liaison O-H est :
s (O-H) = 3600 cm-1.
La fréquence d'absorption de la liaison C-N de l'aniline apparaît vers s (C-N) = 1300 cm-1 ce qui traduit un renforcement de la liaison dû à la
participation à la résonance du doublet de l'azote.
On observe un doublet chez les amines primaires qui est dû au couplage entre les deux vibrateurs N-H. Les vibrations peuvent être symétriques ou
non symétriques.
|
s (cm-1 ) |
3400-3300 |
1600-1490 |
1350-1250 |
|
Vibration |
élongation N-H (simple) |
déformation N-H |
élongation C-N |
On donne ci-dessous deux exemples de spectres.
Exemple 1 : spectre IR de la cyclohexylamine
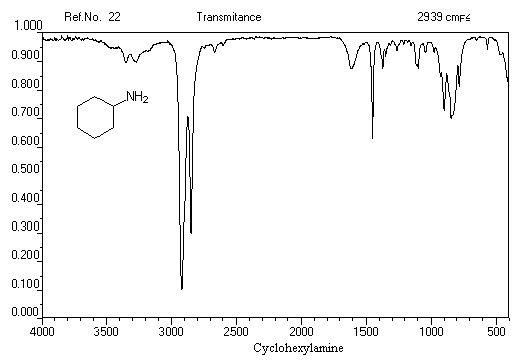
Exemple 2 : spectre IR de la N-méthylaniline
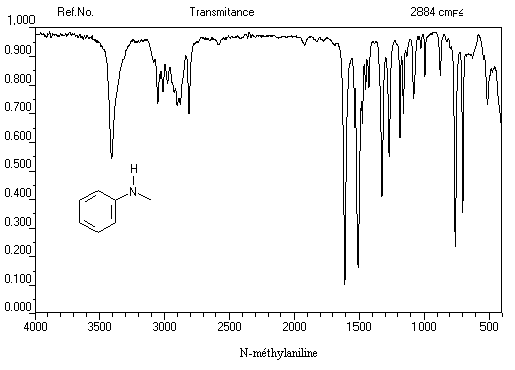
Spectroscopie de RMN
Voici un tableau présentant les déplacements chimiques les plus importants du proton lié à l'azote. On a fait figurer
les amides dans le tableau à titre de comparaison.
|
d (ppm) |
0 - 2 |
2 - 5 |
5 - 9 |
|
Composé |
amines non aromatiques |
amines aromatiques |
amides |
Comme chez les alcools, le proton lié à l'azote est mobile. L'ajout de quelques gouttes d'eau lourde
entraîne le déplacement du pic correspondant.
Un moyen d'identifier les protons liés à l'azote consiste à enregistrer le spectre dans un solvant inerte puis en présence d'acide
trifluoroacétique qui protone l'amine. Le pic du proton lié à l'azote possède un déplacement chimique plus grand dans le cation
que dans l'amine.
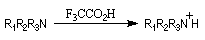
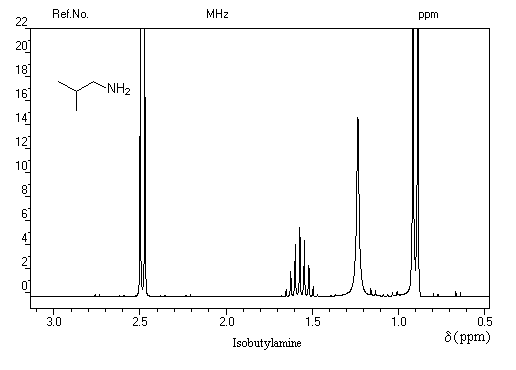
Le spectre de RMN de l'isobutylamine est donné ci-dessous à titre d'exemple. Les protons liés à l'azote donnent un signal large pour un déplacement chimique moyen d = 1,2 ppm (ce déplacement chimique est sujet à variations et il dépend beaucoup des conditions expérimentales car les protons liés à l'azote sont mobiles.) Le signal large est dû aux associations entre les molécules d'amines qui entraînent une multiplication du nombre de fréquences pour lesquelles les protons du groupe amino résonnent. Notons que le couplage entre les protons du groupe amino et les protons du méthylène adjacent n'apparaît pas dans le spectre. Cela est dû au phénomène d'échange chimique.
Le spectre RMN de l'aniline présente un singulet pour d = 3,2 ppm dû aux atomes d'hydrogène du groupe amino et un massif complexe centré sur d = 6,5 ppm correspondant aux atomes d'hydrogène du cycle.
Spectroscopie dans l'ultraviolet et le visible
La spectroscopie dans l'ultraviolet et le visible est surtout utile pour les amines aromatiques. Le spectre ci-dessous est celui de l'aniline.
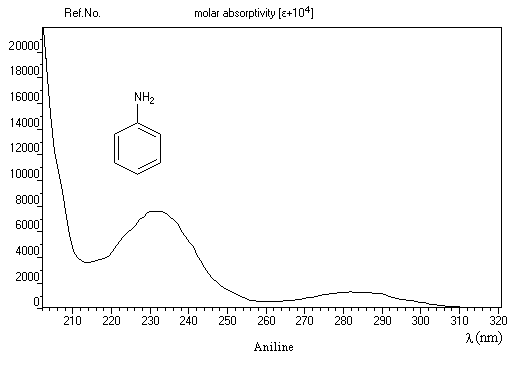
Il est intéressant de comparer les spectres du benzène de l'aniline et de l'ion anilinium. Le tableau ci-dessous résume les
valeurs des maximums d'absorption.
|
Composé |
bande E |
bande B |
|
benzène |
203 nm (e = 7400) |
254 nm (e = 204) |
|
aniline |
235 nm (e = 8600) |
285 nm (e = 1430) |
|
ion anilinium |
203 nm (e = 7500) |
254 nm (e = 169) |
Le groupe -NH2 déplace le maximum d'absorption des bandes B et E du cycle aromatique vers les grandes longueurs d'onde (effet bathochrome) tandis que leur intensité est accrue (effet hyperchrome). Ces effets peuvent être attribués à la conjugaison entre le doublet de l'azote et le cycle. En revanche, l'ion anilinium dans lequel la résonance a disparu, possède
un spectre très comparable à celui du benzène.
Lorsque la conjugaison s'étend sur un plus grand nombre d'atomes comme dans les composés diazoïques, la longueur d'onde du maximum d'absorption peut se trouver dans le domaine visible. Le composé est coloré. L'hélianthine est un composé dont la couleur dépend de l'extension du système conjugué avec le pH.
Propriétés acido-basiques
Basicité
Elle est due au doublet non liant porté par l'atome d'azote. La plupart des amines manifestent des propriétés basiques en solution aqueuse. La réaction prépondérante avec l'eau peu s'écrire :
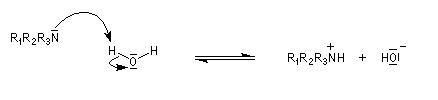
Ainsi qu'on le constate sur le tableau ci-dessous, les valeurs numériques de la constante d'acidité Ka pour le couple ion aminium/amine varient beaucoup d'un couple à l'autre.
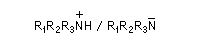
|
Composé |
PhNH 2 |
PyH |
NH 3 |
Me 3N |
MeNH2 |
Me 2NH |
|
pK a |
4,6 |
5,6 |
9,2 |
9,8 |
10,6 |
10,7 |
Expérimentalement, en solution aqueuse, on constate que les amines acycliques sont plus basiques que l'ammoniac. Plus précisément, on observe l'ordre suivant des basicités :
secondaires > primaires > tertiaires
Cet ordre n'est pas facile à rationaliser car les écarts observés ont une faible amplitude. Plusieurs effets possédant le même ordre de grandeur se superposent : électroniques, stériques, et surtout solvatation.
En série cyclique, la situation est plus compliquée. Ainsi, l'aniline est 100 000 fois moins basique que la cyclohexylamine : pKa (CyNH3+/CyNH2) = 9,6 ; pKa (PhNH3+/PhNH2) = 4,6. On interprète habituellement ce résultat par le fait que le doublet non liant de l'aniline est moins disponible dans cette amine aromatique que dans la cyclohexylamine du fait de la délocalisation électronique dans le premier cas. Cependant, cet effet n'est pas isolé ; la solvatation joue aussi un rôle important.
Le cas des amines hétérocycliques aromatiques est aussi un sujet délicat.
- Dans la pyridine, le doublet de l'azote n'est pas impliqué dans le système aromatique. La pyridine est basique.
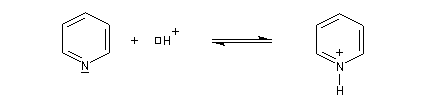
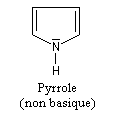
- En revanche, dans le pyrrole, le doublet participe à la conjugaison au sein d'un cycle aromatique. Le pyrrole ne manifeste pas de propriétés basiques.
La basicité intrinsèque, peut être déterminée en phase gazeuse
en utilisant les techniques de résonance cyclotronique ionique. Elle peut être très différente de celle observée en présence d'un solvant. J. I. Brauman a montré dans les années 70 que la basicité intrinsèque des amines croit régulièrement avec le degré de substitution de l'azote. Il est amusant de constater que des mesures analogues faites sur l'acidité des amines montrent qu'elle varie également dans le même sens !
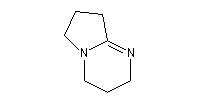
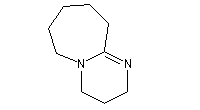
Les amines tertiaires ci-dessous sont fréquemment utilisées pour promouvoir des réactions d'élimination E2. Ce sont des bases encombrées, non nucléophiles ce qui permet de limiter les réactions de substitution. Dans DBN et DBU, l'un des atomes d'azote forme un système conjugué avec une cétimine ce qui renforce la basicité.
Ces bases sont beaucoup moins fortes que les amidures.
|
|
|
|
|
1,5-diazabicyclo[4.3.0]non-5-ène
(DBN) |
1,8-diazabicyclo[5.4.0]undec-7-ène
(DBU) |
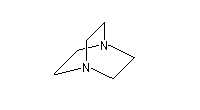
1,4-diazabicyclo[2.2.2]octane
(DABCO) |
La transformation suivante, utilisée dans la synthèse de la cantharidine permet de passer d'un alcène à un diène. L'addition de dibrome sur la double liaison éthylénique est suivie d'une double réaction d'élimination E2.
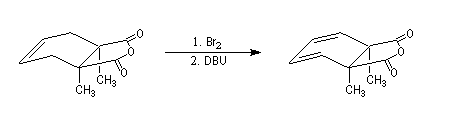
|
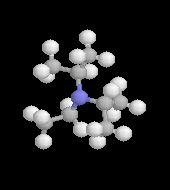
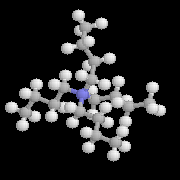
|
L'image de gauche représente la molécule de N, N-diisopropyléthylamine en core appelée base de Hunig. Elle peut remplacer la triéthylamine comme capteur de protons dans de nombreuses applications. Elle présente en outre plusieurs avantages par rapport à cette dernière :
- elle possède une nucléophilie très faible ;
- elle est difficilement alkylable ;
- elle peut être facilement recyclée par distillation azéotropique et peut être extraite sous forme de son acide conjugué en phase aqueuse. Ce recyclage réduit les coûts de fabrication dans les synthèses industrielles.
|
Les propriétés basiques des amines se manifestent par la formation de composés ioniques avec l'acide picrique. Ces composés, facilement cristallisables, peuvent être purifiés aisèment. Ils servent à identifier les amines par repérage de leur température de fusion.
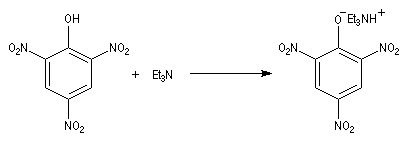
Un mode opératoire est décrit à la référence [2].
La basicité des amines est mise à profit pour leur extraction d'un milieu réactionnel.
- en milieu aqueux, en présence d'acides forts, on obtient des sels d'aminium solubles dans l'eau ;
- il est possible d'opérer en milieu non aqueux avec des solutions de HCl dissous dans l'éther. Dans ce cas, le chlorhydrate d'aminium précipite en milieu inorganique.
Amidures
Les amines primaires et secondaires sont des acides de Brönsted très faibles pKa > 30. Contrairement aux alcools qu'on peut déprotoner, en quantité certes très faible,
dans l'eau, la réaction n'est pas envisageable avec les amines. Les amines peuvent être déprotonées en milieu non aqueux par des bases très fortes telles que le butyllithium nBuLi.
On prépare ainsi plusieurs bases lithiées. Par exemple le diisopropylamidure de lithium (iPr)2N-Li+, noté traditionnellement LDA.
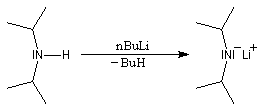
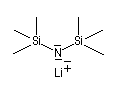
Les bases dérivées de l'hexaméthyldisiliazane sont fréquemment utilisées. Ce dernier peut être préparé en faisant réagir l'ammoniac avec le chlorure de triméthylsilyle.
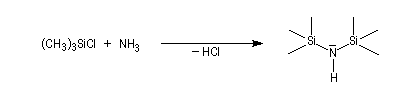
L'aptitude du silicium à stabiliser une charge négative en a est bien connue. On prépare ainsi le LHMDS.
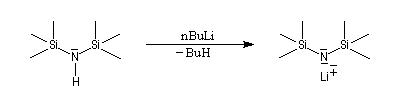
Le tableau ci-dessous regoupe quelques bases usuelles. Les bases analogues sodiques et potassiques de LHMDS sont également utilisées lorsqu'on souhaite éviter la présence du
cation lithium. Un exemple est fourni par la réaction de Wittig stéréosélective Z en présence d'ylures non stabilisés.
|
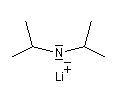
|
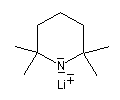
|
|
|
LDA pK = 36 (solvant DMSO) |
LTMP pK = 37 (DMSO) |
LHMDS pK = 30 (DMSO) |
On utilise généralement le LDA à basse température, typiquement - 78 °C. Cette base possède plusieurs atouts :
- solubilité en milieu organique, même à basse température dans des solvants comme le THF ;
- grande force (pKa = 36) ;
- nucléophilie très faible du fait de l'encombrement important des groupes isopropyles.
Les bases fortes précédentes sont utilisées dans la préparation d'énolates cinétiques de composés carbonylés. Un exemple est fourni par la préparation de l'énolate cinétique d'une cétone a-méthylée avant son piégeage sous forme d'éther d'énol silylé.
Une autre méthode pour déprotoner les amines consiste à coupler la réaction acide-base avec la réduction de l'ion H+ grâce à un métal alcalin.
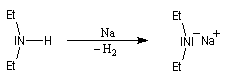
Signalons que le sodium se dissout dans l'éthylamine liquide pour donner des paires ions-électrons solvatés comme dans l'ammoniac liquide.
Complexation
Formation de complexes
Les amines sont des bases de Lewis et, à ce titre, forment de nombreux complexes avec les ions métalliques des éléments de transition. Les amines simples sont des ligands comparables à l'ammoniac. Une diamine comme l'éthylène diamine (diamino-1,2-éthane, symbolisée par én) possède deux points d'ancrage. C'est un ligand bidente (en anglais : bidentate.)
L'augmentation très importante de la constante de stabilité observée quand on remplace l'ammoniac par l'éthylènediamine trouve son origine dans l'effet entropique. Dans la réaction de formation du premier complexe, le nombre de particules n'est pas modifié.
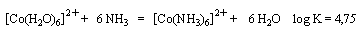
En revanche on constate un accroissement du nombre de particules dans la réaction de formation du complexe avec l'éthylènediamine.
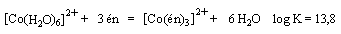
La constante de formation du second complexe est beaucoup plus grande dans le second cas. Ce phénomène porte le nom d'effet chélate (du grec chele : pince, en référence aux ligands polydentes.)
|
|
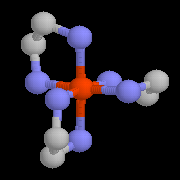
L'image de gauche représente un complexe du cobalt (III) utilisant l'éthylènediamine comme ligand [Co(en)3]2+. Ce complexe, préparé pour la première fois par A. Werner en 1912 présente la particularité d'être chiral.
On trouve un complexe azoté du cobalt dans la partie centrale de la molécule de vitamine B 12 dont la
synthèse totale a été effectuée par R. B. Woodward et A. Eschenmoser [48]
|
Le mélange racémique des énantiomères I et II peut être dédoublé [32].
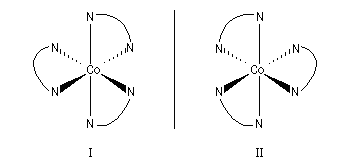
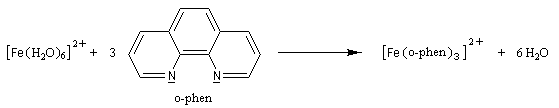
Le complexe entre le fer (II) et l'orthophénantroline est utilisé comme indicateur redox sous le nom de ferroïne.
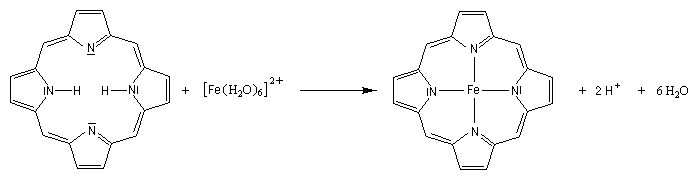
La myoglobine et l'hémoglobine comportent un complexe porphyrine-fer (II) appelé hème dans lequel on trouve quatre unités pyrrole. La réaction suivante traduit la complexation d'un ion Fe (II) par une porphyrine.
Des complexes organométalliques chiraux tels que Fe (S,S) PDP, ont été mis au point assez récemment (catalyseur de White et Chen).
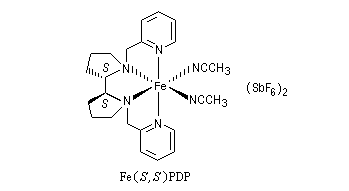
Ils permettent l'oxydation en alcools de liaisons C-H non activées sur des atomes de carbone tertiaire.
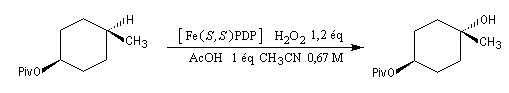
Piv désigne le groupe triméthylacétique (pivalique), un groupe protecteur de la fonction alcool (voir [17]).
Complexation des organométalliques
Les amines primaires et secondaires sont déprotonées quantitativement par les organomagnésiens et les organolithiens. Un exemple évoqué plus haut est la préparation de la base lithiée LDA. Les amines tertiaires sont
compatibles avec les organométalliques et sont parfois utilisées comme solvant de ces composés. La tétraméthyléthylènediamine (TMEDA) forme des complexes stables, solubles en milieu organique avec les organolithiens. La complexation du lithium accroit fortement la polarité de la liaison organométallique
et exalte le caractère de carbanion du lithien.
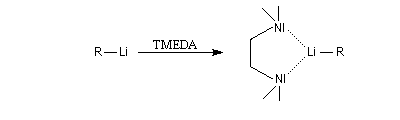
Le butyllithium complexé par la TMEDA est un agent basique particulièrement puissant.
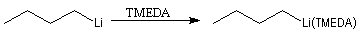
Ce type d'organométallique est capable de déprotoner le ferrocène.
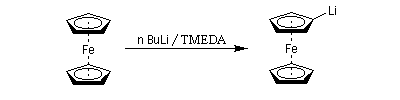
Les organométalliques forment des complexes colorés avec l'orthophénantroline et la bisquinoléine ce qui permet d'effectuer leur dosage par la méthode de Watson et Eastham.
Les organolithiens chélatés par des ligands chiraux comme la spartéine permettent des réactions de déprotonation énantiosélectives.
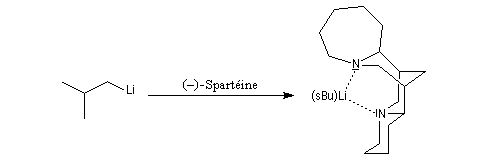
Cryptands
Les cryptands sont des macrohétérobicycles. On peut les considérer comme des structures prolongeant à trois dimensions celles des polyéthers macrocycliques de type couronne synthétisés par C. J. Pedersen en 1967. Ils sont capables de
former des complexes stables et sélectifs avec un certain nombre de cations durs tels que les alcalins et alcalino-terreux. Ces complexes sont appelés cryptates.
|
![Cryptand [2,2,2]](images11/cryptand.gif)
|
L'image de gauche représente le cryptand [2,2,2] synthétisé par J.-M. Lehn et son équipe en 1969. Il forme des complexes 1-1 avec
des cations métalliques que J.-M. Lehn a appelé cryptates du grec cryptos caché. La stabilité du complexe dépend de la nature du cation.
Elle varie dans l'ordre :
K+ > Rb+ > Na+ > Li+ > Cs+.
Li+ et Cs+ sont respectivement trop petit et trop gros pour être complexés de façon efficace. J.-M. Lehn a obtenu le prix Nobel de chimie conjointement avec les Américains D. J. Cram et C. J. Pedersen en 1987.
|
Citons quelques propriétés remarquables des cryptands :
- La solubilité dans l'eau du sulfate de baryum est multipliée par 10 000 en présence du cryptand [2,2,2].
- Les cryptands sont aussi des agents de transfert de phase. La densité de charge d'un cation camouflé au sein d'un cryptate est fortement diminuée tandis que le caractère lipophile de l'ensemble est considérablement accru. L'anion associé peut être véhiculé
en phase organique est faiblement lié au cryptate. De ce fait, sa réactivité s'en trouve exaltée. On peut ainsi réaliser des substitutions en utilisant l'ion fluorure comme nucléophile.
- L'aptitude de certains cryptands à complexer les cations alcalino-terreux a été mise à profit pour extraire le strontium (II) radioactif d'organismes vivants.
- Signalons pour terminer une réaction remarquable réalisée par J. L. Dye et son équipe de l'Université du Michigan en 1974. En dissolvant du sodium en présence de cryptand [2,2,2] ces auteurs ont préparé un composé ionique de couleur jaune d'or contenant l'anion Na- !
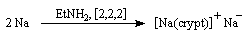
L'étude des propriétés des complexes macrocycliques constitue un domaine en plein développement et ouvre la voie à une chimie dans laquelle la notion de reconnaissance joue un rôle déterminant et qu'on appelle chimie supramoléculaire [18].
Alkylation
Bilan de l'alkylation d'Hofmann
La méthode a priori la plus simple pour alkyler l'atome d'azote d'une amine consiste à la faire réagir avec un dérivé halogéné.
Avec une amine primaire ou secondaire il y a substitution d'un atome H par un groupe alkyle. On obtient donc en principe l'amine appartenant à la classe immédiatement supérieure. Avec une amine
primaire, le bilan théorique s'écrit :
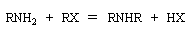
Cependant HX étant un acide fort, il est dissocié en solution :
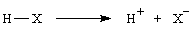
Il faut donc tenir compte des équilibres acido-basiques suivants :
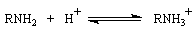
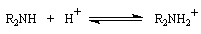
Ces équilibres diminuent le rendement de la réaction en privant l'amine de son caractère nucléophile.
On peut s'affranchir de cette difficulté en utilisant une base peu nucléophile comme l'ion carbonate qui réagit avec les ions H+ formés.
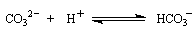
Avec une amine tertiaire on obtient un halogénure d'ammonium quaternaire.
Mécanisme
Il s'agit d'une réaction de substitution utilisant comme substrat le dérivé halogéné et l'amine comme réactif nucléophile. Avec un substrat primaire ou secondaire la réaction est de type SN2. Les substrats tertiaires sont peu exploitables en raison de la réaction concurrente d'élimination. L'amine peut en effet jouer le rôle de base.
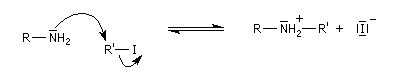
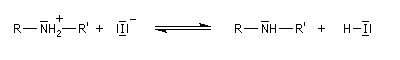
Intérêt et limitations de la réaction
L'alkylation directe des amines avec un dérivé halogéné ne constitue généralement pas une très bonne méthode synthétique car l'amine alkylée réagit à son tour avec le réactif. On obtient donc un mélange de produits qu'il faut ensuite séparer. Une méthode simple et douce d'alkylation des amines est l'amination réductive des aldéhydes et des cétones.
La perméthylation d'Hofmann ou méthylation exhaustive, consiste à méthyler tous les sites possibles de l'amine. On utilise l'iodométhane comme agent alkylant. Avec ce substrat, la réaction est facilitée par le caractère d'excellent nucléoguge de l'ion iodure et il ne peut y avoir d'élimination. De plus, l'iodométhane est liquide à la température ordinaire. En présence d'un excès d'iodométhane, on obtient l'ion ammonium quaternaire.
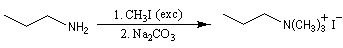
La quantité de matière n d'iodométhane nécessaire pour atteindre l'ion ammonium permet de déterminer la classe de l'amine.
|
n (mol) |
3 |
2 |
1 |
|
Classe d'amine |
primaire |
secondaire |
tertiaire |
Par exemple, dans le cas ci-dessous, la réaction nécessite trois équivalents d'iodométhane. On en déduit que l'amine est primaire.
Remarque : la diméthylaniline peut être préparée en utilisant deux moles d'iodométhane pour une mole d'aniline.
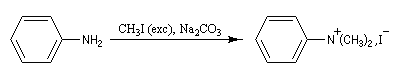
D'un point de vue expérimental, il faut se rappeler que l'iodométhane est un agent alkylant très puissant et de ce fait, il est extrêmement toxique pour l'organisme.
La réaction ci-dessous est extraite de la synthèse de l'acide lysergique (Woodward, 1956 [45]). Elle permet l'introduction d'une chaîne latérale en a du groupe carbonyle après bromation régiosélective dans cette position.
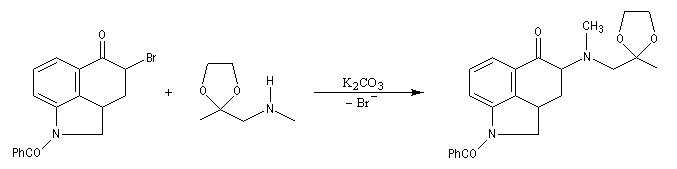
Alkylation de l'ammoniac
L'alkylation de l'ammoniac constitue une méthode de synthèse des amines primaires. Puisque l'ammoniac est très soluble dans l'eau, on peut utiliser des solutions aqueuses
très concentrées. Le réactif est alors en grand excès par rapport à l'halogénure et la polyalkylation devient négligeable. La synthèse de la 1-méthyl-2-phényléthylamine illustre cette manière de procéder.
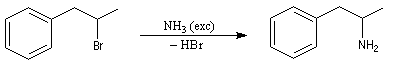
|
|
Le terme amphétamine est le nom donné au mélange racémique de deux énantiomères de la 1-méthyl-2-phényléthylamine. Ils ont une structure voisine d'un neurotransmetteur : l'adrénaline. Ce type de composé agit comme stimulant du système nerveux central. Les composés de la famille des amphétamines ont été utilisé par certains sportifs dans le but d'améliorer leurs performances. Il sont sans doute à l'origine de la mort dramatique du champion du monde cycliste Tom Simpson dans l'ascension du mont Ventoux lors du Tour de France 1967.
|
Substitution nucléophile aromatique
L'atome d'azote d'une amine primaire ou secondaire peut substituer un halogène porté par un cycle aromatique fortement désactivé selon un mécanisme d'addition-élimination.
Le 1-chloro-2,4-dinitrobenzène forme des dérivés facilement cristallisables permettant d'identifier les amines [6].
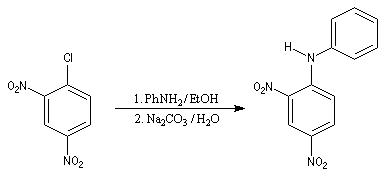
L'atome d'azote d'un amino-acide
est suffisamment nucléophile pour déplacer le fluor du dinitrofluorobenzène ou réactif de Sanger. On peut
ainsi déterminer la position de l'amino-acide N-terminal d'une protéine.
Réactions des ions ammonium quaternaires
Réactions d'élimination à partir des ions ammonium quaternaires
Les ions ammonium quaternaire possèdent un groupe -NR3+ lié à une chaine carbonée. Si l'atome de carbone en b
possède un atome d'hydrogène, une élimination conduisant à un composé éthylénique est possible.
Les amines étant d'assez mauvais nucléofuges (à corréler empiriquement à une basicité élevée) la réaction doit être effectuée en présence d'une base forte à chaud.
L'oxyde d'argent en suspension dans l'eau ou oxyde d'argent "humide", est très utilisé. Son rôle est double :
- C'est un oxyde basique, qui en présence d'eau, est une source d'ions OH- :
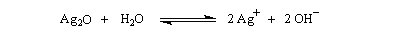
- L'ion Ag+ réagit avec avec I- pour donner de l'iodure d'argent AgI très peu soluble, ce qui décolle cet ion de la paire d'ions formée avec l'ion alkylammonium.
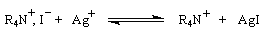
La régiosélectivité de l'élimination suit la règle d'Hofmann. Si deux composés éthyléniques peuvent se former, le composé majoritaire est celui qui possède la double liaison la moins substituée.
Les résultats suivants concernent l’élimination d’Hofmann sur l’iodure de (1-méthylpropyl)-triméthylammonium. Les diastéréo-isomères Z et E du but-2-ène sont très minoritaires par rapport au but-1-ène.
|
Composé |
but-2-ène (Z et E) |
but-1-ène |
|
% |
5 |
95 |
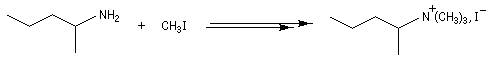
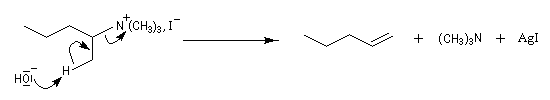
Plusieurs explications ont été avancées pour expliquer la régiosélectivité de l'élimination d'Hofmann. Dans la théorie de l'état de transition variable développée par J. F. Bunnett, la formation du composé le moins substitué
est à mettre en relation avec le fait que -NR3 n'est pas un bon nucléofuge. Rappelons à cet égard la règle empirique corrèlant l'aptitude nucléofuge et la basicité. Les amines ne sont pas des bases très faibles ce sont donc de mauvais nucléofuges.
|
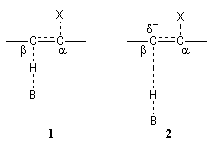
|
Le schéma de gauche représente une illustration de la théorie de l'état de transition variable.
Dans le complexe activé (1)
d'une élimination bimoléculaire E2 l'arrachage de l'atome d'hydrogène par la base B et le départ du nucléofuge X sont synchronisés.
En présence d'un mauvais nucléofuge X, l'arrachage de l'atome d'hydrogène précède le
départ de X. Il en résulte pour le complexe activé (2) l'apparition d'une charge négative sur l'atome de carbone en b qui lui confère un caractère de carbanion.
|
Le mécanisme de l'élimination est de type bimoléculaire E2 mais se rapproche du mécanisme E1cB dans lequel on observe la formation d'un carbanion.
La régiosélectivité est alors déterminée par l'acidité cinétique de l'atome d'hydrogène porté par l'atome de carbone en b.
C'est l'hydrogène le plus dégagé qui est arraché le plus rapidement par la base conduisant au composé éthylénique le moins substitué. Mis à part le cas de certaines éliminations sur les dérivés halogénés, la
crotonisation des aldols en milieu basique procède également de ce mécanisme.
Application de la réaction d'Hofmann à la détermination des structures
A l'époque où l'on ne disposait pas du puissant moyen d'analyse que constituent les méthodes spectrales, la détermination de la structure des molécules s'effectuait par voie chimique. L'élimination d'Hofmann a été mise à profit pour déterminer la structure de molécules complexes notamment des alcaloïdes. La nature des composés éthyléniques issus de l'élimination d'Hofmann peut être déduite de l'analyse
des produits de coupure par ozonolyse. Examinons un exemple. Soit à déterminer la position du groupe méthyle dans l'amine cyclique
ci-dessous qui est un dérivé de la pipéridine.
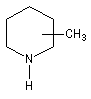
Par une suite de méthylations et d'éliminations d'Hofmann on obtient un
composé éthylénique (A) dont l'ozonolyse en milieu réducteur fournit du méthanal et du butanedial. On peut remonter à la structure de l'amine
en considérant successivement les réactions ci-dessous :
- ozonolyse ;
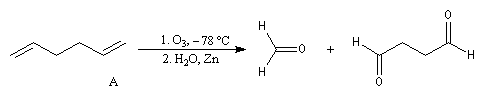
- méthylation ;
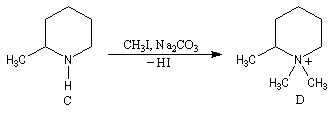
- élimination d'Hofmann ;
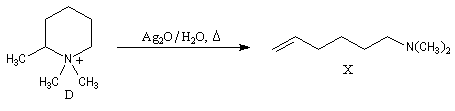
- méthylation ;
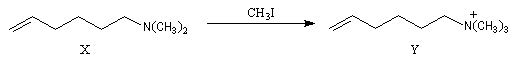
- élimination d'Hofmann ;
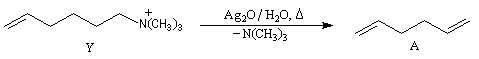
Application de la réaction d'Hofmann en synthèse
La réaction d'Hofmann est utilisée dans la synthèse de doubles liaisons éthyléniques.
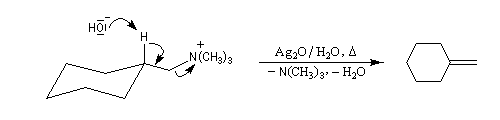
Le méthylènecyclohexane peut aussi être obtenu par réaction de Wittig.
L'exemple suivant concerne les deux dernières étapes de la synthèse du barrelène par H. E. Zimmerman (1960).
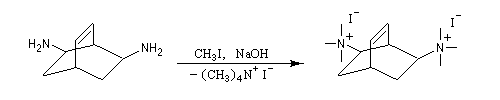
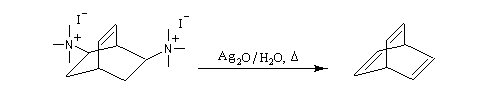
La réaction a permis, à A. C. Cope en 1953 la préparation du (E)-cyclooctène [23].
Utilisation des ions ammonium quaternaires dans les réactions par transfert de phase
Les ions ammonium quaternaires sont des amphiphiles. Ils comportent une
partie apolaire et une partie ionique. Cette structure originale leur permet d'être solubles en milieu aqueux sous forme ionique
et d'exister en milieu organique engagés dans des paires d'ions faiblement liés. Lorsqu'une réaction implique des espèces anioniques,
l'une des difficultés est de disposer d'anions suffisamment réactifs dans la phase organique. Une solution à ce problème consiste à véhiculer les
anions dans cette phase grâce à un contre-ion positif qui partage son affinité entre la phase aqueuse et la phase organique. Ces ions transporteurs
sont recyclés au fur et à mesure de la réaction, c'est pourquoi on parle de catalyse par transfert de phase.
Le schéma ci-dessous résume les principaux équilibres dans le cas d'une réaction de substitution :
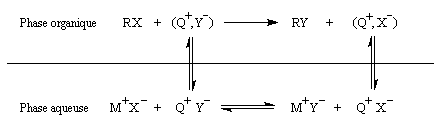
|
|
La catalyse par transfert de phase a été découverte par le chimiste polonais M. Makosza en 1965. Elle consiste à réaliser une réaction dans un milieu diphasé organique / aqueux en présence d'un catalyseur
pouvant se partager entre les deux milieux, comme un ion ammonium quaternaire R4N+ un éther couronne ou un cryptand.
Cet ion peut véhiculer les anions en phase organique où ils acquièrent une plus grande réactivité. La réaction peut être réalisée à température assez basse sans utiliser de solvant dipolaire aprotique.
Un site [14] est spécialement consacré à ce type de catalyse.
|
L'exemple suivant concerne l'alkylation d'un composé carbonylé en a du carbonyle.
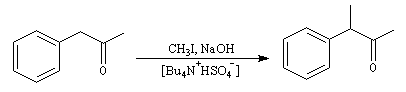
Un autre exemple d'utilisation de ce type de catalyse est l'oxydation de l'acétate d'isoeugénol en vaniline.
On peut aussi synthétiser des éthers en milieu biphasé organique/aqueux en utilisant les ions OH- comme base en présence d'un ammonium quaternaire comme agent de transfert de phase.
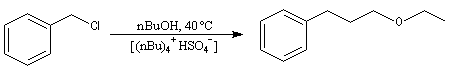
Il est possible de réaliser des synthèses énantiosélectives en utilisant des ions ammonium quaternaires chiraux comme le sel de cinchonidinium suivant obtenu à partir de l'alcaloïde cinchonidine
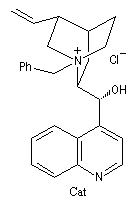
Dans l'exemple suivant, ce catalyseur est utilisé dans une réaction d'époxydation d'un dérivé de la benzoquinone.
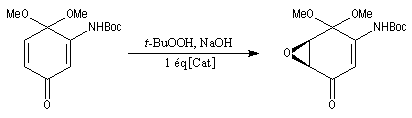
Il s'agit d'une étape d'une synthèse récente d'un antibiotique, la manumycine C. L'excès énantiomérique est supérieur à 99,5 %.
Acylation
Bilan
Il s'agit de la réaction entre une amine primaire ou secondaire et un agent acylant : halogénure d'acyle, anhydride d'acide, acide carboxylique. Elle fournit un amide.
On observe une réaction du même type avec l'ammoniac. La présence d'au moins un atome d'hydrogène sur l'azote est essentielle. C'est la raison pour laquelle les amines tertiaires ne peuvent être acylées.
Acides carboxyliques
La réaction entre une amine et un acide carboxylique engage l'essentiel des réactifs sous forme de sel d'aminium inerte vis à vis de la réaction d'acylation puisque cet ion a perdu tout caractère nucléophile.
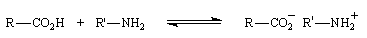
La réaction n'est donc généralement pas utilisée sauf dans quelques cas particuliers. La synthèse du phtalimide s'apparente à la réaction précédente mais le composé azoté est l'ammoniac.
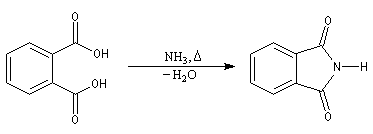
Ce composé est utilisé dans la synthèse de Gabriel des amines primaires.
Chlorures d'acyles et anhydrides
La réaction entre une amine primaire ou secondaire et un chlorure d'acyle ou un anhydride permet la préparation des amides. La méthode la plus ancienne est celle de Schotten-Baumann. La réaction est effectuée en milieu aqueux avec une solution diluée d'ions hydroxyde OH- dont le rôle est de neutraliser l'acide formé. L'amine est suffisamment nucléophile
pour que la réaction concurrente des ions hydroxyde vis à vis de l'halogénure d'acyle soit négligeable.
Au début du siècle, A. Einhorn a modifié le protocole initial en remplaçant les ions hydroxyde par la pyridine.
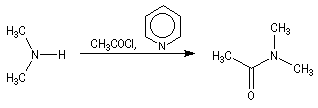
Les amines aromatiques subissent la même réaction :
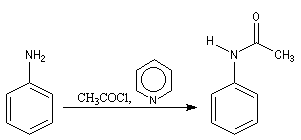
l'acétanilide est un solide incolore de point de fusion 114 °C, [4].
Plus récemment W. Steglich et L. M. Litvinenko ont introduit la diméthylaminopyridine (DMAP) qui s'est révélé un catalyseur extrêmement efficace dans ce genre de réactions.
Mécanisme dans le cas des halogénures d'acyles
Il s'agit d'un mécanisme par addition-fragmentation. La réaction ressemble à celle vue avec les alcools. L'étape cinétiquement déterminante est la formation de l'intermédiaire tétraédrique.
Ce dernier subit une fragmentation quasiment irréversible avec départ de l'ion halogénure.
- addition nucléophile ;
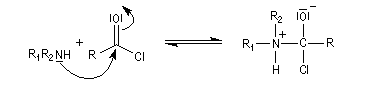
- fragmentation de l'intermédiaire tétraédrique ;
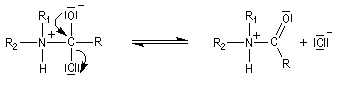
- l’ion acylaminium est ensuite déprotoné par une base comme la pyridine.
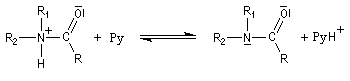
Le rôle de la pyridine est double :
- elle neutralise l'acide formé ;
- il s'agit d'un catalyseur nucléophile qui forme un adduit intermédiaire (I) avec le chlorure d'acyle.
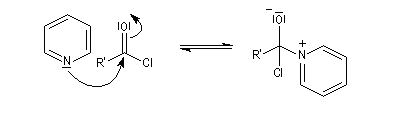
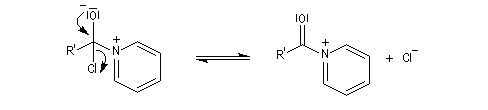

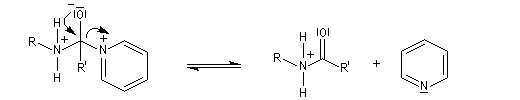
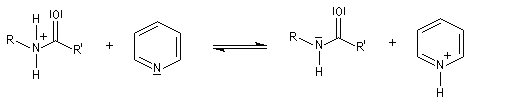
Notons que l'acylation des amines tertiaires s'arrête au stade de l'ion acylaminium intermédiaire car il n'y a pas d’atome d’hydrogène sur l'azote. Les deux étapes sont alors équilibrées. En présence d'un excès d'eau, l'ion redonne l'amine et l'acide carboxylique parent du chlorure d'acyle.
Catalyse par la DMAP
La N, N-diméthylaminopyridine (DMAP), est utilisée pour accélérer les réactions d'acylation des alcools et des phénols ainsi que dans certaines hydrolyses. Il s'agit d'un catalyseur très efficace même dans les réactions intramoléculaires difficiles comme les macrolactonisations et les macrolactamisations. La DMAP est également utilisée comme
catalyseur de la réaction de Baylis-Hillman.
|
|
A la température ordinaire la DMAP se présente sous la forme d'un solide blanc, fondant à 111,6 °C. Il s'agit d'un composé toxique, à manipuler avec précautions. La DMAP est largement utilisée au laboratoire et en synthèse comme
catalyseur nucléophile.
|
Il s'agit d'une catalyse nucléophile dont le principe est le même qu'avec la pyridine. La plus grande efficacité de la DMAP par rapport à cette dernière, peut être interprétée par le fait que l'azote pyridinique possède une charge négative élevée comme en
témoignent les formes mésomères suivantes :
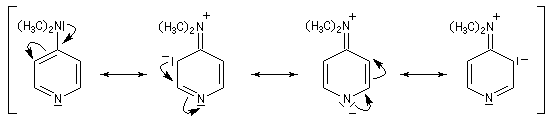
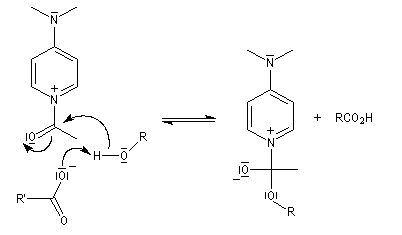
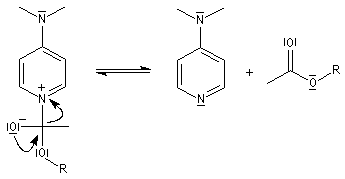
Le mécanisme de catalyse par la DMAP est donné ci-dessous.
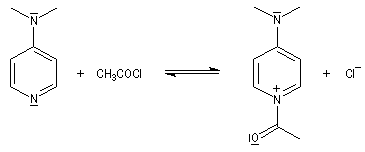
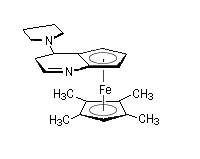
Dérivés chiraux de la DMAP
|
|
Des dérivés chiraux de la DMAP utilisant un groupement ferrocénique ont été préparés très récemment [31]. Ils servent de catalyseurs
dans différents types de transformations :
|
Protection régénération
Les amides peuvent être hydrolysés en milieu acide ou en milieu basique dans des conditions assez dures. La transformation d'un groupe amino en groupe acétamido constitue un moyen de protection du groupe amino.
Exemple : la synthèse de l'acide amino-3-benzoïque peut être effectuée par oxydation du groupe méthyle de la 3-méthylaniline mais les amines aromatiques étant très sensibles à l'oxydation, la réaction directe est impraticable. Il faut au préalable effectuer la protection du groupe amino :
- protection de la fonction amine ;
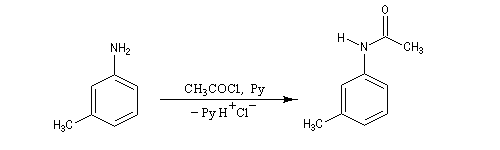
- oxydation du groupe méthyle ;
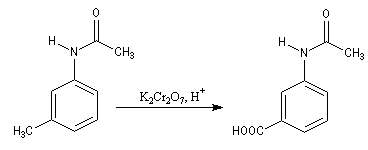
- régénération du groupe amino par hydrolyse de l’amide en milieu acide ou basique.
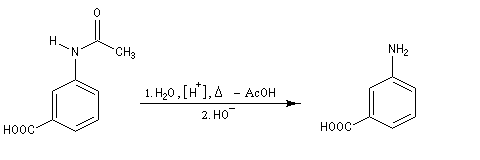
Le groupement N-t-butoxycarbonyle introduit à partir du chlorure de t-butoxycarbonyle, un chlorure d'acyle, ou de l'anhydride correspondant, est utilisé comme groupe
protecteur des fonctions amines primaires et secondaires. La réaction sert couramment à protéger un aminoacide dans une synthèse peptidique.
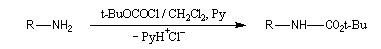
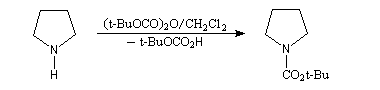
Le groupe est stable vis à vis des bases. La fonction amine est régénérée par hydrolyse acide.
Synthèse du Nylon 6-6
Le Nylon 6-6 est un polyamide artificiel. Sa synthèse a été réalisée par le chimiste américain W. H. Carothers (du Pont de Nemours).
Dans l'industrie, on le prépare par réaction entre l'acide hexanedioïque (acide adipique) et le diamino-1,6-hexane (hexaméthylène diamine) à 280 °C.
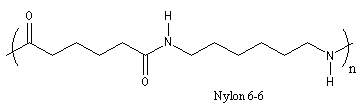
Une préparation plus commode au laboratoire consiste à remplacer l'acide adipique par le chlorure d'acyle correspondant [2]. Un polyamide
voisin est appelé Nylon 6. Il est préparé par polymérisation du caprolactame.
|
|
Le nylon est utilisé comme fibre textile ainsi que dans la fabrication de pièces mécaniques (paliers, engrenages etc.) Parmi les nombreuses anecdotes concernant l'origine du nom choisi par
Carothers, l'une d'elles probablement apocryphe, est à mettre en relation avec le fait qu'à l'époque une bonne partie de la soie provenait du Japon. Nylon
serait constitué des premières lettres de la phrase : Now You're Lost Old Nippons.
|
D'autres polyamides ont acquis une grande importance ces dernières années : les polyaramides dont le représentant le plus connu est le kevlar. Ce dernier allie une grande résistance mécanique et une masse volumique faible. On l'utilise
dans la fabrication des gilets pare-balles.
Synthèse de Bischler-Napieralski
L'acylation de la b-phényléthylamine par un chlorure d'acyle est la première étape d'une réaction permettant de préparer les quinolidines substituées connue sous le nom de réaction de Bischler-Napieralski. Il s'agit d'une synthèse mettant en jeu plusieurs étapes qui possède plusieurs points communs avec la réaction de Vilsmeier-Haack.
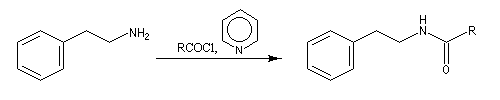
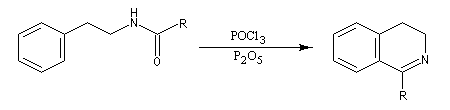
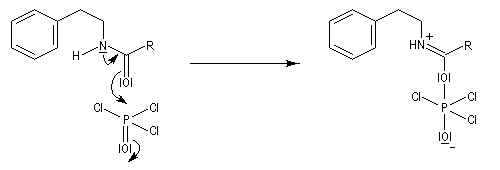
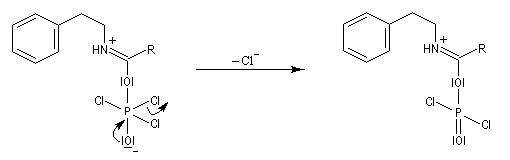
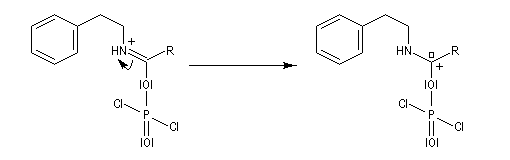
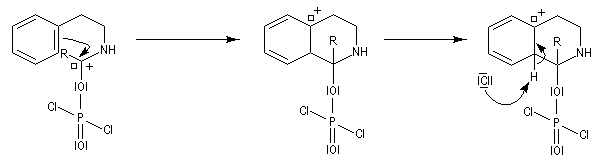
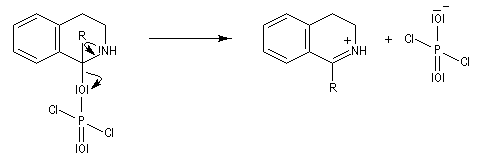
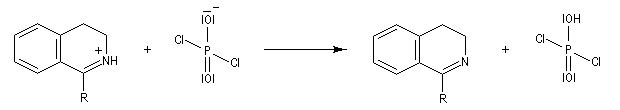
La réaction de Bischler-Napieralski a été appliquée avec succès à la synthèse de la papavérine alcaloïde quinolidinique extrait du pavot (papaver somniferum). Ce composé est utilisée en médecine comme antispasmodique.
|

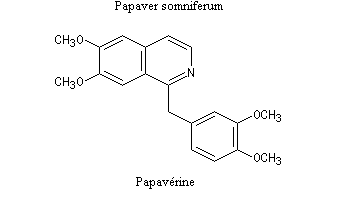
|
Lorsqu'on incise les capsules de pavot somnifère (papaver somniferum), celles-ci exsudent un liquide laiteux. Après séchage, il conduit à une résine brune qui constitue l'opium.
L'opium contient de nombreux alcaloïdes : codéine, papavérine, laudanosine, morphine.
La morphine (du grec Morphée : Dieu du sommeil) est l'alcaloïde le plus important de l'opium qui en contient jusqu'à 23 %. Isolée par F. Sertüner, sa structure a été établie en 1925 par J. M. Gulland, R. Robinson et C. Schöpf. La première synthèse de la morphine (racémique) a été réalisée en 1953 par J. M. Gates. Il s'agissait d'une synthèse linéaire comportant 29 étapes pour un rendement total de 0.0014 % ! [20].
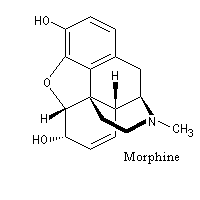
|
Le schéma de la synthèse est donné ci-dessous.
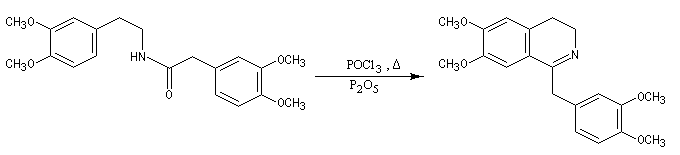
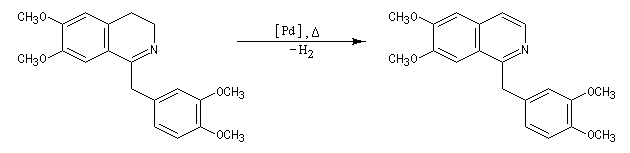
Sulfonylation
Bilan
La réaction entre un halogénure d'acide sulfonique et une amine primaire ou secondaire fournit une sulfonamide.
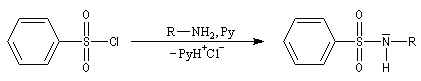
Les sulfonamides issus d'amines primaires possèdent un atome d'hydrogène mobile. Elles réagissent en milieu basique pour donner un composé ionique soluble en milieu aqueux.
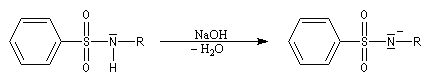
Cette réaction est à la base du test de
qui permet la distinction des trois classes d'amines.
Test de Hinsberg
Ce test est basé sur la solubilité de la sulfonamide quand elle existe en milieu basique. Un mode opératoire pour la réalisation de ce test est détaillé à la référence [3]. Les
résultats sont résumés dans le tableau ci-dessous.
|
Classe de l’amine |
primaire |
secondaire |
tertiaire |
|
Solubilité sulfonamide |
oui |
non |
pas de sulfonamide |
Réactions avec les composés carbonylés
Imines
Synthèse des imines et des ions iminium
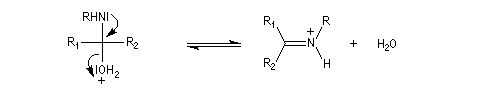
L'addition d'une amine primaire sur un composé carbonylé conduit, par une réaction équilibrée, à un amino-alcool peu stable. La réaction est catalysée en milieu acide. Cependant le pH ne doit pas être trop bas sinon l'amine est protonée et l'addition nucléophile
ne se produit plus.
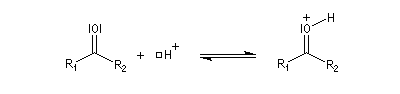
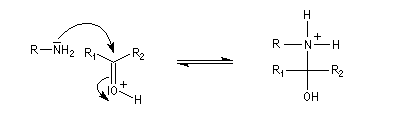
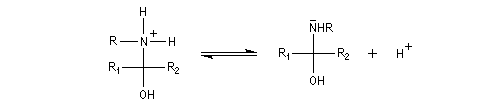
Les amino-alcools se déshydratent facilement en milieu acide pour donner des imines encore appelées bases de Schiff en souvenir du chimiste d'origine allemande Ugo Schiff qui les
a étudiées [64].
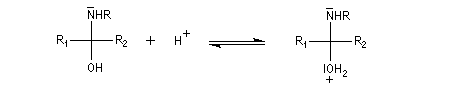
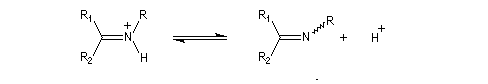
Une autre voie d'accès aux imines est la réaction de Staudinger (aza-Wittig.)
Les imines peuvent être regardées comme les analogues azotés des composés carbonylés. Elles possèdent comme ces derniers une liaison double polarisée. On peut donc prévoir qu'elles donneront lieu à des réactions d'addition.
Les imines dérivant de l'ammoniac sont instables. Si l'on fait réagir le méthanal avec l'ammoniac on obtient un composé
cristallin de couleur blanche : l'hexaméthylènetétramine (HMTA). Au cours de cette réaction, l'aldimine intermédiaire, instable, ne
peut pas être isolée.
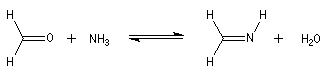
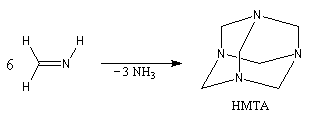
|
|
Le Tétraazatricyclo[1,1,3,3,7,7]décane ou hexaméthylènetétramine(HMTA) est un composé curieux rappelant la
molécule d'adamentane. A la température ordinaire, il se présente sous la forme de cristaux blancs, solubles dans l'eau, qui fondent à 280 °C.
L'HMTA est utilisé en médecine comme antiseptique sous le nom d'urotropine (étym : qui fait bouger l'urée) en raison de ses propriétés diurétiques.
Il s'agit d'une source de cation iminium qui est utilisée dans la formylation de composés aromatiques activés (réaction de Duff) [46]
|
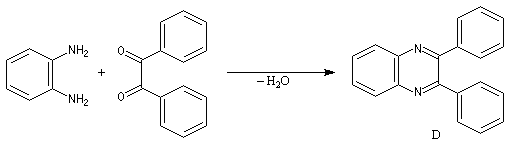
La réaction de déshydratation est favorisée lorsque le composé obtenu est fortement conjugué comme dans la synthèse de la diphénylquinoxaline D [6].
Les amines secondaires donnent des ions iminium.
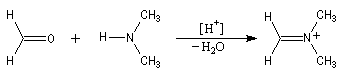
Benzodiazépines
Les benzodiazépines sont des composés psychoactifs, anxiolytiques et hypnotiques. Elles sont utilisés notamment en anesthésie. L'analyse rétrosynthétique des benzodiazépines [1,4] montre qu'on peut les obtenir en créant une imine et un amide.
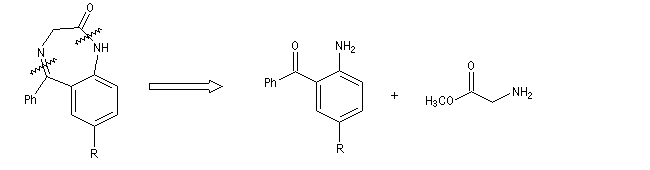
L'amidification est souvent réalisée en utilisant l'aminolyse d'un ester comme le glycinate de méthyle. L'étape de cyclisation est la formation de l'imine. L'exemple ci-dessous constitue une étape de la synthèse du diazepam.
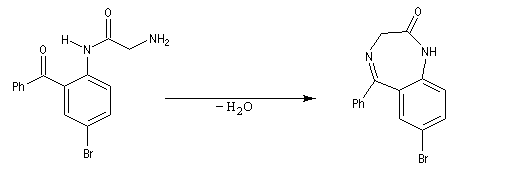
Les autres benzodiazépines [1,4] sont obtenues à partir d'amino-benzophénone judicieusement substituées.
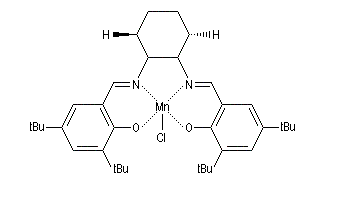
Ligand salen, complexes de Jacobsen
La synthèse du composé salen-H2 à partir de l'aldéhyde salicylique et de l'éthylènediamine, constitue un autre exemple de réaction de ce type. Cette imine joue le rôle de ligand vis à vis du cobalt (II) dans un complexe capable de fixer le dioxygène de façon réversible.
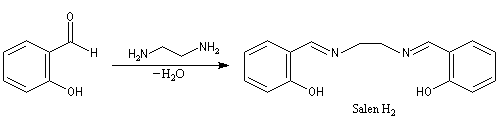
Ce type de complexes fait, à l'heure actuelle, l'objet de recherches approfondies car on pense qu'ils pourraient servir de composés modèles pour la préparation de sang artificiel. Une synthèse du composé salen-H2 est décrite dans [11].
Des complexes métalliques utilisant des ligands salen diversement substitués, ont été synthétisés assez récemment par E. Jacobsen à Harvard. Ce sont des catalyseurs efficaces de plusieurs réactions intéressantes en synthèse asymétrique :
Réduction des imines
La formation d'une imine à partir d'un composé carbonylé, suivie de son hydrogénation in situ, constitue une méthode d'alkylation douce des amines appelée amination réductive.
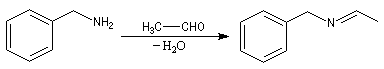
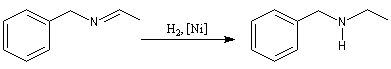
Lorsque la réaction est effectuée en utilisant l'ammoniac comme composé azoté, il s'agit d'une synthèse d'amine primaire à partir d'un composé carbonylé.
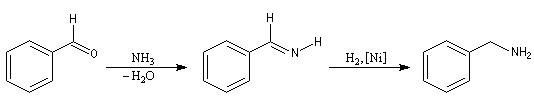
Le tétrahydroborate de sodium NaBH4 peut être utilisé comme agent réducteur mais se pose le problème de la réduction du composé carbonylé. Un excellent réactif permettant la réduction des imines est NaCNBH3. Utilisé à pH 6-7, il ne réduit pas le groupe carbonyle des aldéhydes et des cétones, ce qui permet l'amination réductive [40]. En revanche, ce réactif réduit les carbonylés à pH 3-4. Le contrôle du pH est donc important dans cette réaction.
Addition des organométalliques
L'addition d'un organomagnésien sur une imine substituée suivie d'une hydrolyse de l'adduit constitue une méthode de
synthèse d'amines secondaires.
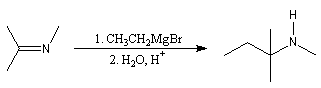
Réaction d'Eischweiler-Clark
Il s'agit d'une méthylation des amines primaires et secondaires au moyen du mélange méthanal-acide méthanoïque (acide formique). La réaction procède en deux
étapes. Raisonnons dans le cas d'une amine secondaire.
Réaction de Mannich
La réaction de Mannich consiste en l'addition d'un atome de carbone nucléophile sur un ion ion iminium formé in situ. Le réactif nucléophile est l'énol d'un composé carbonylé ou d'un phénol. La réaction est facilitée lorsque l'ion iminium
est issu de la condensation entre le méthanal et une amine primaire ou secondaire car dans ce cas l'atome de carbone du réactif
est très électrophile.
Le schéma rétrosynthétique est le suivant :
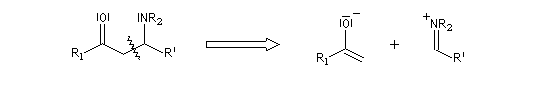
Examinons un exemple : la suite des réactions est la suivante :
- formation de l'ion ion iminium (sel d' Eschenmoser) ;
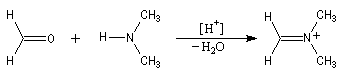
- équilibre de tautomérie entre le composé carbonylé et son l'énol ;
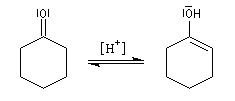
- réaction d'addition entre l'énol et l'ion ion iminium.
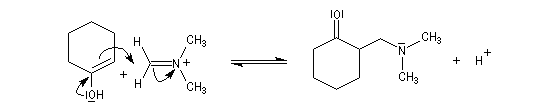
Les composés obtenus, appelés bases de Mannich, peuvent subir par chauffage une élimination
conduisant à une a-énone.
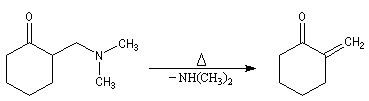
La réaction précédente est donc particulièrement utile pour la préparation de ce type de composés qui constituent des substrats
de départ dans plusieurs synthèses.
La réaction de Mannich a été utilisée dans de nombreuses synthèses de composés appartenant à la famille des alcaloïdes. L'exemple suivant est une étape de la synthèse de la strychnine par R. B. Woodward [38]
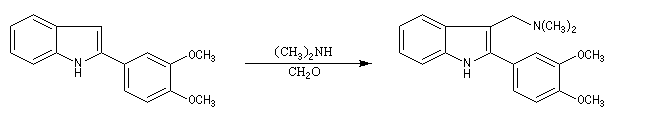
Application de la réaction de Mannich à la synthèse de la tropinone
La tropinone est une molécule bicyclique dont on retrouve le squelette dans de nombreux alcaloïdes. On peut
l'obtenir par dégradation de l'atropine présente à l'état naturel dans la belladone.
|
|
L'hyosciamine est l'un des principaux alcaloïdes d'une plante herbacée appelée atropa belladonna (Belladone). Ses décoctions possèdent la propriété de dilater la pupille de l'oeil. Elles étaient utilisées au XVIII ème siècle par les femmes italiennes pour augmenter la profondeur de leur regard. Le nom de Belladone vient de bella donna qui signifie jolie femme en italien. Le mélange racémique de l'hyosciamine et de son énantiomère est appelé atropine. Il est utilisé comme antidote de certains gaz de combat car il agit comme inhibiteur des récepteurs parasympathiques. Son mécanisme d'action s'explique par sa fixation sur les récepteurs de l'acétylcholine dans le système nerveux central et périphérique. C'est le médicament de référence contre le malaise vagal.
|
La synthèse de la tropinone fut réalisée par le chimiste allemand R. Willstäter en 1901 (prix Nobel de chimie 1915, [27]). On la considère généralement comme
l'une des premières synthèses d'une molécule complexe. Elle comportait 15 étapes et le rendement global était inférieur
à 1 %.
Au cours de son étude remarquable des alcaloïdes qui devait le rendre mondialement célèbre et lui valoir le prix Nobel de chimie en 1947, le chimiste
britannique R. Robinson (Université d'Oxford, [28]) en a donné une synthèse en 1917 qui est devenue un classique. Elle est basée sur une double réaction de Mannich. Il s'agit d'un exemple de réaction domino (ou réaction en cascade) car les évènements se déroulent les uns à la suite des autres sans qu'il soit nécessaire d'isoler un composé intermédiaire [43].
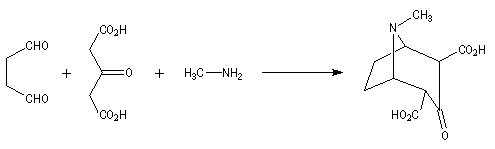
Le mécanisme de la réaction est donné ci-desssous :
La réaction entre le succinaldéhyde et la méthylamine fournit un aminoalcool qui se cyclise spontanément.
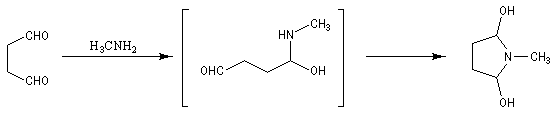
Le composé obtenu perd de l'eau en milieu acide pour conduire à un ion iminium.
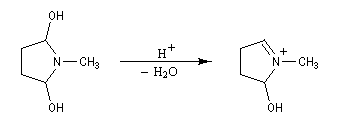
L'énol du diacide réagit sur l'ion iminium.
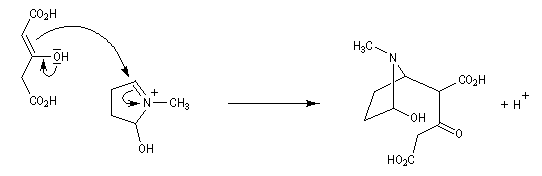
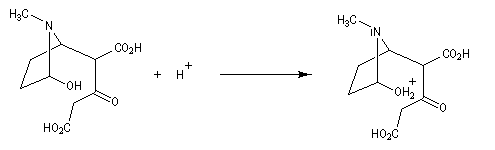
Formation à nouveau d'un ion iminium.
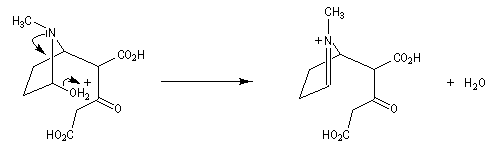
Suivi d'une deuxième réaction de Mannich.
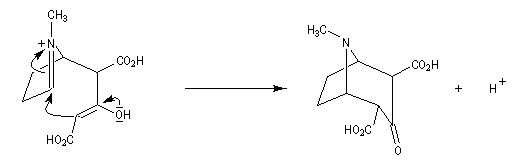
Le b-céto acide formé subit une décarboxylation thermique.
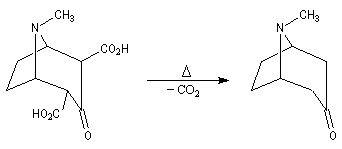
En milieu biologique les alcaloïdes de la famille de la tropinone comme la cocaïne ou la scopolamine sont synthétisés selon une voie
comparable. On donne le nom de synthèse biomimétique à l'ensemble de procédés synthétiques
dont l'objectif est de reproduire en laboratoire les réactions observées dans le domaine vivant.
Enamines
Origine
Les énamines peuvent être considérées comme les analogues azotés des énols et des éthers d'énols. Les énamines possédant un atome d'hydrogène sur l'azote (énamines primaires et secondaires) sont peu stables et se réarrangent en imines.
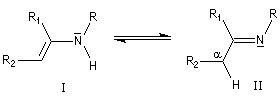
L'équilibre entre énamine (I) et imine (II) constitue un exemple de tautomérie dont le mécanisme est comparable à celui de la tautomérie céto-énolique.
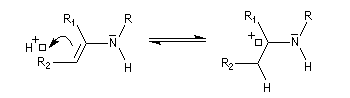
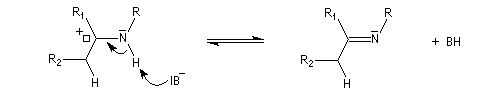
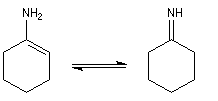
L'exemple ci-dessous concerne une énamine primaire.
Un autre exemple est celui de l'adénine qui présente deux formes tautomères : énamine (I) et imine (II). Dans la molécule d'ADN, l'appariement avec la thymine s'effectue par des liaisons hydrogène impliquant la forme (I).
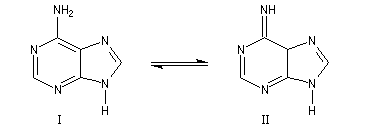
Les énamines tertiaires ne possèdent pas d'atome d'hydrogène lié à l'azote et ne peuvent pas donner lieu à l'équilibre de tautomérie.
Synthèse des énamines
On prépare les énamines par réaction entre une amine secondaire et un composé carbonylé possédant un atome d'hydrogène sur l'atome de carbone en a du carbonyle en présence d'un catalyseur comme l'APTS. Le mécanisme suivant concerne la synthèse d'une énamine
tertiaire en présence d'un catalyseur noté BH+.
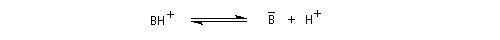
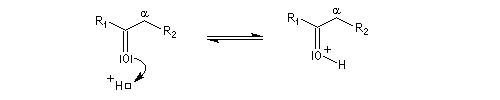
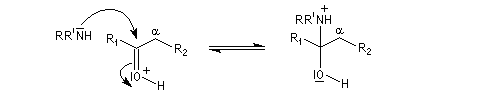
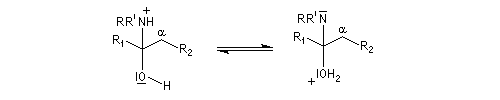
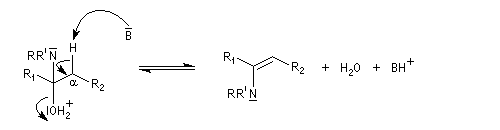
L'équilibre n'est pas favorable au produit. Une méthode couramment utilisée pour déplacer l'équilibre, consiste à éliminer l'eau du milieu réactionnel par distillation azéotropique en utilisant un décanteur de Dean-Stark. On trouvera des protocoles opératoires aux références [7] et [29].
Les énamines sont stables en milieu basique et peuvent être utilisées dans certains cas comme
groupement protecteur de la fonction carbonyle. Le traitement de l'énamine par un excès d'eau en présence d'une quantité catalytique d'acide fournit l'amine et le composé carbonylé parents.
L'exemple ci-dessous concerne la réaction entre la cyclohexanone et la pyrrolidine.
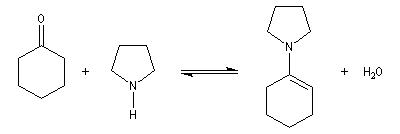
Les énamines sont des intermédiaires très utilisés en synthèse organique. Comme le montrent les formes mésomères ci-dessous, une charge négative peut se développer sur l'atome de carbone situé en b de l'azote.
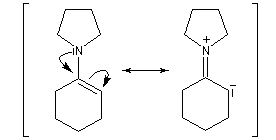
Les énamines sont des nucléophiles qui peuvent réagir avec des substrats électrophiles acylant ou alkylant.
Acylation des énamines
La réaction entre une énamine et un agent acylant assez réactif comme un chlorure d'acyle permet la synthèse de systèmes dicarbonylés 1, 3. Un mode opératoire
de la réaction suivante se trouve à la référence [12].
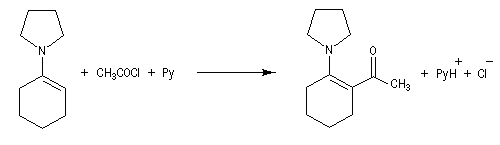
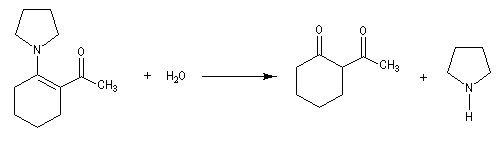
La réaction ci-dessous est la première étape de la synthèse de Oppolzer du longifolène.
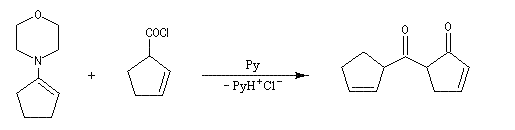
Alkylation des cétones
L'alkylation des composés carbonylés, (notamment celle des cétones qui est la plus pratiquée), sur l'atome de carbone en a
du carbonyle pose un problème de régiosélectivité. La réaction par union directe de la cétone et d'un réactif alkylant comme l'iodométhane fournit un mélange de cétone mono et polysubstituée. Pour pallier cette difficulté
plusieurs méthodes ont été proposées. L'une d'elles, mise au point par le chimiste américain d'origine belge G. Stork, consiste à utiliser une énamine comme intermédiaire.
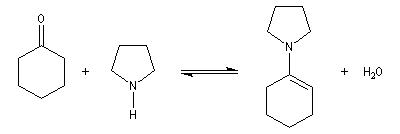
L'énamine réagit avec un équivalent de dérivé halogéné pour fournir un ion iminium.
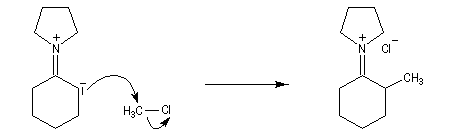
Ce dernier, traité par l'eau, conduit à la cétone alkylée.
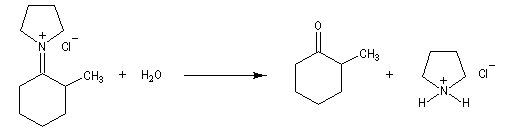
L'ion iminium (I) ne possède pas d'atome de carbone nucléophile. Le problème de la suralkylation ne se pose pas. La technique est également applicable avec des agents alkylants suffisamment réactifs comme les halogénures allyliques ou benziliques.
Avec des agents alkylants de moyenne réactivité comme l'iodure d'éthyle c'est surtout la N-alkylation qui prédomine.
Une autre méthode d'alkylation régiosélective des cétones consiste à mettre à profit les propriétés des éthers de silyle.
Régiosélectivité
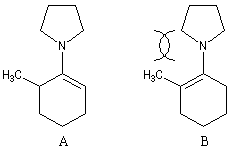
La réaction entre la méthylcyclohexanone et la pyrrolidine fournit l'énamine possédant la liaison double la moins substituée (A) à l'exclusion de son isomère (B). La régiosélectivité de l'élimination est donc opposée à celle qu'on aurait si la règle de Zaytsev était suivie.
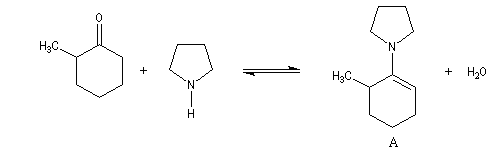
L'examen des molécule (A) et (B) fournit l'explication de la régiosélectivité observée. La conjugaison entre le doublet de l'atome d'azote et la double liaison impose que les atomes impliqués soient dans un même plan. Cette condition n'est pas réalisée dans (B) du fait de la forte répulsion entre le groupe méthyle orienté de façon pseudo-axiale et un groupe méthylène du cycle [41].
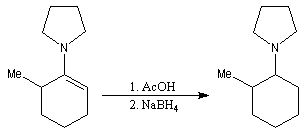
Réduction des énamines
Les énamines peuvent être réduites par hydrogénation catalytique. Le tétrahydroborate de sodium NaBH4 ne réagit pas
directement avec elles. En revanche ce réactif réduit rapidement les ions iminium obtenus en traitant l'énamine en milieu acide.
Nitrosation
Formation de l'électrophile
La nitrosation est la réaction entre une amine et l'acide nitreux HNO2. Ce dernier est un composé instable vis à vis de sa dismutation en NO3- et NO. Il est préparé dans le milieu réactionnel en acidifiant une solution de nitrite de sodium par l'acide chlorhydrique. La véritable entité électrophile est le cation nitrosonium
NO+ qui est impliqué dans les équilibres suivants :
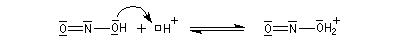
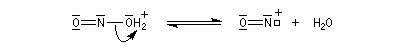
On peut donner une description de l'ion NO
+ en utilisant la méthode de la mésomérie. Elle met en évidence l’azote électrophile.
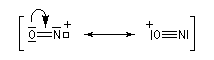
La nature du produit de réaction entre un cation NO+ et une amine, dépend de la classe de l'amine.
Amines secondaires
On obtient une N-nitrosoamine.
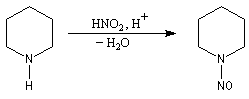
Les N-nitrosoamines sont des composés cancérigènes. Un exemple de synthèse est celui de la diphénylnitrosamine [6].
Amines primaires
Il se forme un ion diazonium.
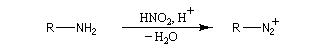
- Les
ions diazonium aliphatiques sont très peu stables car le diazote est un excellent nucléofuge. On obtient un carbocation susceptible de donner lieu à plusieurs réactions selon la nature des réactifs présents dans le milieu réactionnel.
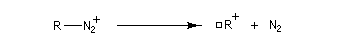
Notons que ces sels de diazonium
sont explosifs à l'état solide.
- Les ions diazonium aromatiques donnent lieu à de nombreuses réactions qui sont étudiées dans un chapitre particulier.
Substitution électrophile sur les amines aromatiques
Activation, régiosélectivité
L'aniline réagit beaucoup plus vite que le benzène dans les réactions de substitutions électrophiles.
Le groupe -NH2 est activant et oriente en ortho-para.
Bromation
La bromation de l'aniline peut s'effectuer très facilement sans catalyseur. Le groupe amino est tellement activant qu'il suffit de mélanger l'aniline et une solution aqueuse de brome, pour obtenir immédiatement un précipité blanc de tribromoaniline.
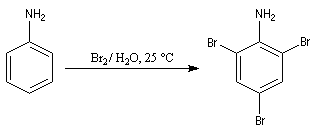
On peut réaliser une monobromation en procédant de façon indirecte. On commence par préparer un amide : le N-phényléthanamide (acétanilide). En ce qui concerne le rapport ortho/para, le groupe acétamido est moins activant et aussi plus encombrant que le groupe amino, on obtient le parabromoacétanilide (pF = 167 °C) dont l'hydrolyse fournit le composé recherché.
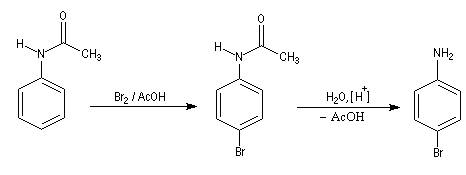
Nitration
La nitration directe de l'aniline est impossible car l'acide nitrique oxyde le groupe amino. Pour s'affranchir de cette difficulté, on utilise un groupe protecteur.
- On commence par préparer un amide : le N-phényléthanamide par réaction entre l'aniline et le chlorure d'éthanoyle, ce qui permet la protection du groupe amino.
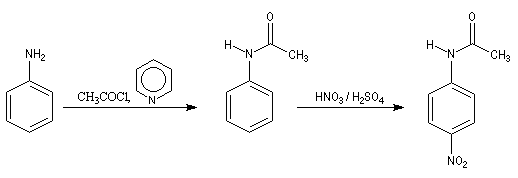
- On effectue ensuite la nitration du N-phényléthanamide. Il s'agit d'une substitution électrophile sur un cycle benzénique présentant déjà un substituant. Le groupe acétamido est activant. Il oriente la substitution en ortho et para. Des deux isomères qui peuvent a priori se former, le dérivé para est majoritaire car la position ortho est plus encombrée que la position para.
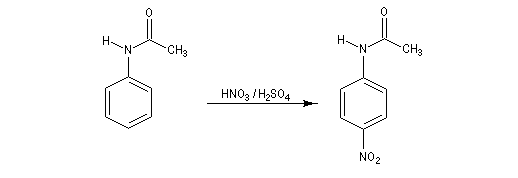
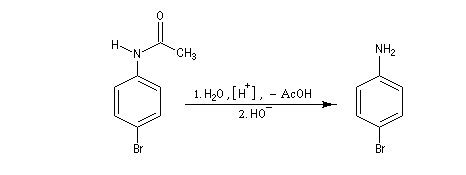
- Il ne reste plus qu'à hydrolyser l'amide en milieu acide ou basique afin de régénérer le groupe amino. La 4-nitroaniline se présente à la température ordinaire comme un solide de couleur jaune (pF = 148 °C.)
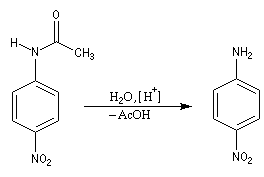
Réaction des amines tertiaires aromatiques avec l'acide nitreux
Avec les amines tertiaires aromatiques, l'acide nitreux en milieu acide conduit à une substitution électrophile sur le cycle. L'entité électrophile est l'ion nitrosonium :
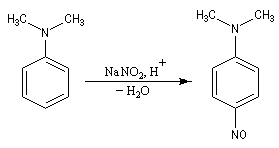
le mécanisme est le suivant :
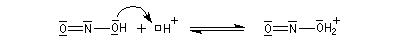
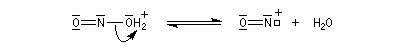
Comme on l'a vu plus haut, la structure de l'ion NO
+ peut être décrite par méthode de la mésomérie. Elle met en évidence l’azote électrophile.
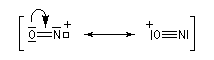
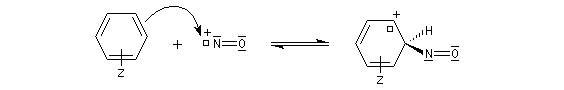
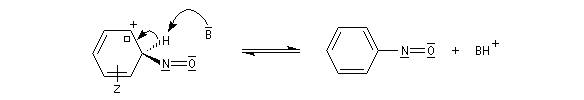
Rappelons qu'avec les amines primaires, l'action de l'acide nitreux conduit à union diazonium. Avec les amines secondaires, on obtient des N-nitrosoamines.
Un mode opératoire est décrit à la référence [6].
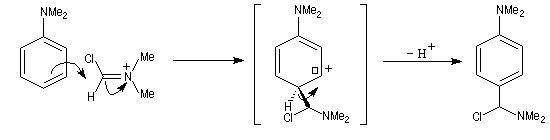
Formylation de Vilsmeier-Haack
La réaction de Vilsmeier-Haack constitue une méthode de formylation des amines aromatiques N, N-disubstituées et de certains hétérocycles comme le pyrrole. On peut la regarder comme une extension de la réaction de Mannich.
La préparation du réactif de Vilsmeier est donnée ci-dessous.
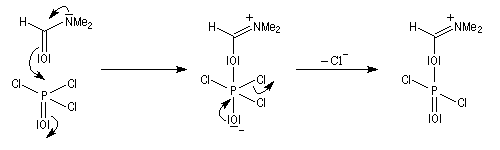
La force motrice de la réaction est la formation d'une liaison P-O de grande énergie de liaison.
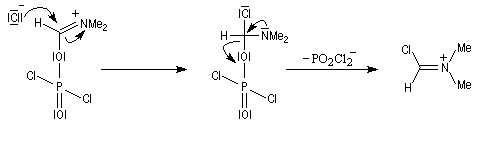
L'ion iminium n'est pas un électrophile très puissant. La réaction a lieu essentiellement avec les composés aromatiques activés.
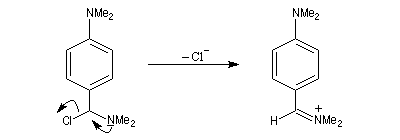
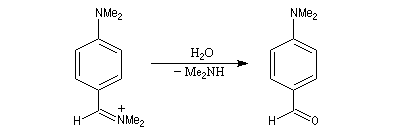
Oxydation des amines
Oxydation des amines tertiaires
Les amines sont des composés assez sensibles à l'oxydation. Les produits de réaction dépendent de la classe de l'amine et de la nature de l'oxydant utilisé. La réaction la plus importante concerne les amines tertiaires. Les oxydants utilisés sont le mCPBA, peroxyde d'hydrogène ou encore l'acide peroxymonosulfurique (acide de Caro).
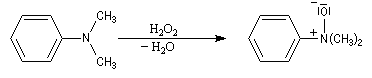
Notons que certains oxydes d'amines sont utilisés comme agents d'oxydation. Le N-oxyde de N-méthylmorpholine (NMO) est utilisé comme cooxydant dans la syn-dihydroxylation vicinale des composés éthyléniques par le tétroxyde d'osmium.
Propriétés des oxydes d'amines
Les réactions importantes des oxydes d'amines sont étudiées dans un chapitre particulier :
Oxydation de l'aniline
L'oxydation de l'aniline dépend de l'agent oxydant utilisé :
- Avec CrO3, on obtient la benzoquinone.
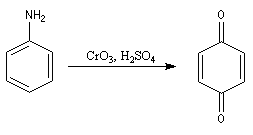
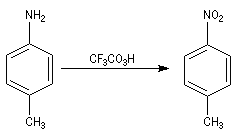
- On peut aussi utiliser un peroxyacide comme CF3CO3H, le groupe amino est oxydé en groupe nitro.
A. Streitwieser Jr, C. H. Heathcock - Introduction to Organic Chemistry, Macmillan Publishing Co.
F. A. Carey, R. S. Sunberg Advanced Organic Chemistry, 5 Ed. Springer (2007)
J. March - Advanced organic chemistry, 6 Ed. Wiley Interscience (2007)
Paul Wyatt, Stuart Warren - Organic Synthesis : Strategy and Control J. Wiley (2007)
Robert Burns Woodward, Architect and artist in the World of molecules. Ed. by Otto Theodor Benfrey and Peter J. T. Morris
P. Laszlo - Logique de la synthèse organique. Cours de l'Ecole Polytechnique, Ellipses, 1993.
P. Atkins - General Chemistry, Scientific American Books W. H. Freeman and Co.
J. Koolman, K. H Röhm - Atlas de biochimie, Médecine & Sciences, Flammarion.
P. Caubère - La catalyse par transfert de phase et son utilisation en chimie organique, Masson 1982.
Organic Synthesis Highlights V, Edited by Hans-Günther Schmalz and Thomas Wirth, J. Wiley 2003.
![]()















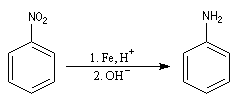










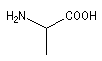
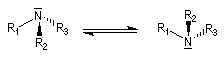

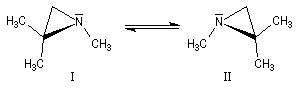
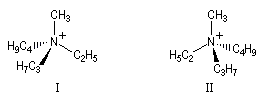
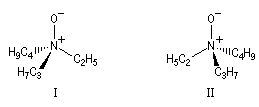
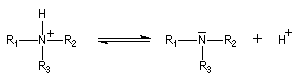






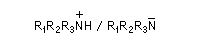
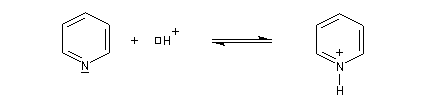




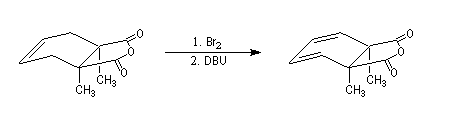

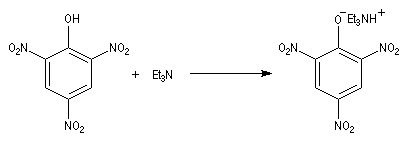
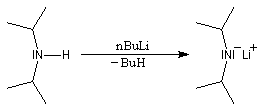
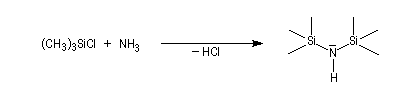
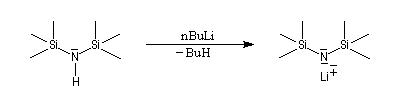
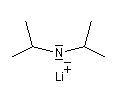
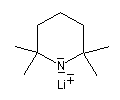

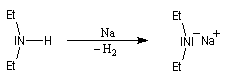

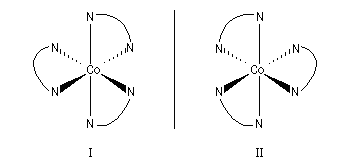



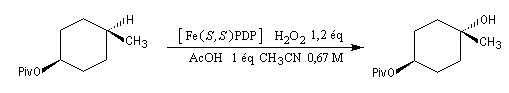

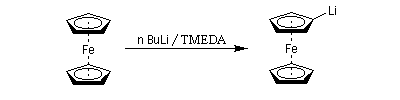
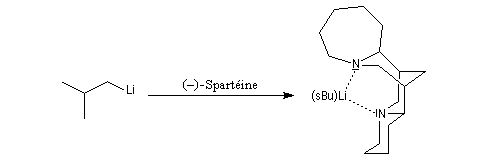
![Cryptand [2,2,2]](images11/cryptand.gif)